|
La Constante de disociación o Kd es definida en termodinámica química como la relación matemática que se establece a partir de las concentraciones de los compuestos químicos que se forman en una reacción de disociación al alcanzar su punto de equilibrio. Producto destacadoSi un compuesto de formula Ax By se disocia según la reacción la constante de disociación Kd se expresa mediante la siguiente relación de concentraciones (en moles por litro): A menudo, la constante de disociación también se formula por pKd siendo
Ejemplo: constante de disociación del aguaLa constante de disociación del agua, expresada por Ke (Kw en inglés), es la constante de reacción asociada a la reacción química de autoprotolisis:
Los productos de ésta reacción son los iones oxonio (o iones hidronio) y los hidroxidos. En el estado de equilibrio químico, y en el caso de disoluciones diluidas, el Ke corresponde al producto de las concentraciones en iones, que en el caso de condiciones normales de temperatura y presión, cumplen la relación:
Esta reacción del agua ocurre de manera natural y espontánea, de manera que en el agua a presión atmosférica se encuentran tanto moléculas de agua como iones en una relación de concentraciones acorde con la Ke específica a cada temperatura:
Categoría: Magnitudes químicas |
||||||||||||||||||||||||||||||||||||
| Este articulo se basa en el articulo Constante_de_disociación publicado en la enciclopedia libre de Wikipedia. El contenido está disponible bajo los términos de la Licencia de GNU Free Documentation License. Véase también en Wikipedia para obtener una lista de autores. |





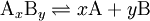
![K_{d} = \frac{[A]^x \times [B]^y}{[A_x B_y]}](images/math/f/a/7/fa734f7c67752b156fc481a917e07f30.png)


