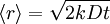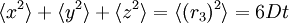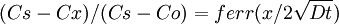|
La difusión es un proceso físico irreversible, en el que partículas materiales se introducen en un medio que inicialmente estaba ausente de ellas aumentando la entropía del sistema conjunto formado por las partículas difundidas o soluto y el medio donde se difunden o disolvente. Normalmente los procesos de difusión están sujetos a la Ley de Fick. La membrana permeable puede permitir el paso de partículas y disolvente siempre a favor del gradiente de concentración. La difusión, proceso que no requiere aporte energético es frecuente como forma de intercambio celular. Producto destacado
Tipos de difusiónLos distintos tipos de difusión pueden ser moderados usando la ecuación de la difusión. La difusión es el movimiento de partículas de un área en donde están en alta concentración a un área donde están en menor concentración hasta que estén repartidas uniformemente. La difusión no solamente incluye difusión de partículas, sino todo fenómeno de transporte ocurrido en sistemas termodinámicos bajo la influencia de fluctuaciones térmicas. La difusión es el proceso a través del cual el sistema de velocidad termodinámica en un equilibrio termodinámico local regresa a equilibrios termodinámicos globales, a través de homogenización de valores de sus parámetros intensos. Desplazamiento de difusiónEl desplazamiento medio de una partícula debido a la difusión puede ser descrito por la siguiente fórmula: Donde k indica el número de componentes del movimiento, es decir, si la dirección del movimiento se define con 1, 2 o 3 componentes (x, y o z). D es el coeficiente de difusión de las partículas y t es tiempo. Para los sistemas tridimensionales la ecuación previa sería: . Difusión sustitucionalÉste tipo de difusión, llamada también difusión por mecanismo de vacantes, consiste en el movimiento de los átomos en estructuras cristalinas; dichos movimientos se generan principalmente a causa de la energía térmica de los átomos, aunque también existen otros factores que pueden contribuir a este tipo de difusión como lo suelen ser las impurezas en el cristal. Difusión intersticialEn cambio este tipo de difusión se produce cuando los átomos entrantes son más pequeños que los existente en la red cristalina. Las ley que rige la difusión es la Ley de Fick otra forma para encontrar la correlacion de dificion entre atomos es sacar la derivada por la hipotenusa entre el radio de cierta medida, entre los caracteres de un punto polar en la primera cara de cff; por la integral de dicha ecuacion. 1ª Ley de Fick (estado estacionario)Se produce cuando todos los átomos entrantes son salientes, cuando no hay agregación de materia.
Siendo D la difusividad:
Q= Energía de activación para la difusión R= cte de los gases T= Temperatura absoluta (K) 2ª Ley de Fick (estado no estacionario)
D= difusividad Co= concentración inicial Cx= concentración final Cs= concentración superficial t= tiempo x= distancia desde la superficie Separación isótopa
Difusión a través de membranas biológica
Véase también
Enlaces externos
be-x-old:Дыфузія Categoría: Fisicoquímica |
|
| Este articulo se basa en el articulo Difusión publicado en la enciclopedia libre de Wikipedia. El contenido está disponible bajo los términos de la Licencia de GNU Free Documentation License. Véase también en Wikipedia para obtener una lista de autores. |