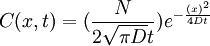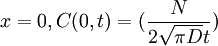|
La célula está cubierta por una superficie externa, conformada principalmente por fosfolípidos y proteínas, denominada membrana celular. Su función es proteger e intermediar en el proceso de transporte de moléculas y sustancias entre el interior y exterior de la célula. Dentro de los procesos de transporte que se llevan a cabo en la membrana se encuentran el proceso de difusión simple y facilitada, a lo cual se le denomina transporte pasivo, y a través de transportadores primarios y secundarios, como transporte activo. El paso de moléculas a través de una membrana debido a una diferencia de concentración, se denomina difusión simple, en este caso el desplazamiento de las moléculas va en la dirección del gradiente de concentración, el cual va de una zona de mayor a menor concentración. El proceso de difusión simple es estudiado a través de las Leyes de Fick, las cuales relacionan la densidad de flujo de moléculas, la diferencia de concentración, el coeficiente de difusión de las moléculas y la permeabilidad de la membrana como variables fundamentales en el proceso de difusión. Con el objetivo de analizar el proceso de difusión simple en las membranas se realizó un breve análisis de la primera y segunda Ley de Fick, para estudiar el comportamiento de las moléculas y las variables que intervienen en el proceso de difusión. Dentro de los resultados obtenidos con el programa se llegó a que, de acuerdo con la primera Ley de Fick, la densidad de flujo es directamente proporcional a la diferencia de concentración y que esta a su vez varía de acuerdo con la molécula que este atravesando la membrana. Además, en relación con la segunda Ley, se evidenció que la concentración relativa en función de las distancias recorridas por las moléculas, describe una distribución gaussiana, en la que a menor tiempo de observación, se alcanza un valor máximo en su pico. Producto destacado
IntroducciónLa membrana celular, en general, se encuentra constituida por fosfolípidos, los cuales están formados por una cabeza polar hidrofílica (fosfato cargado eléctricamente) y dos colas apolares e hidrofóbicas (ácidos grasos). De acuerdo con las propiedades de los fosfolípidos estos se organizan formando una bicapa lípidica, la cual se constituye en una barrera de protección y proceso de intercambio de sustancias con el medio externo. La membrana celular limita el intercambio de moléculas o sustancias, puesto que presenta una permeabilidad selectiva que interviene en los procesos de transporte, los cuales pueden ser de carácter activo o pasivo. Dentro del transporte pasivo se encuentra el paso de moléculas por difusión simple y facilitada (canales o poros), que se da debido a la diferencia de concentraciones en el interior y exterior de la membrana, generando un gradiente de concentración proporcional al flujo neto, razón por la cual no requiere energía adicional. El transporte activo ha diferencia del pasivo, se presenta a través de transportadores, los cuales requieren de energía para transportar moléculas a través de la membrana aún en contra del gradiente de concentración, un ejemplo de ello, son las proteínas que hacen parte de las membranas celulares, estas utilizan la energía proporcionada por el ATP o por los carbohidratos de la membrana para transportar moléculas. Difusión simpleLa difusión es un movimiento aleatorio que depende de la energía térmica de un sistema de partículas y de la diferencia de concentración entre dos regiones, de modo que el flujo neto de partículas de una región de mayor concentración a otra de menor concentración se puede entender como difusión simple o transporte de pasivo de partículas. Cuando este fenómeno se presenta, se evidencia un gradiente de concentración que indica la dirección del flujo, en el cual se desplazan las partículas. En el caso de las membranas celulares, la difusión simple depende de la concentración y del tipo de molécula que va a ser transportada. Las moléculas que pasan a través de la membrana debido a este fenómeno son únicamente los gases (CO2, O2), las moléculas hidrofóbicas (benceno) y las moléculas polares pequeñas (H2O y etanol), puesto que la membrana es permeable a este tipo de moléculas, las cuales además son solubles en su bicapa lípidica. Por otra parte, las moléculas polares grandes (glucosa), los aminoácidos y las moléculas cargadas o iones (H+,Na+,Cl+ y Ca2+) son transportadas a través de la membrana por medio de los diferentes tipos de transportadores. Para el estudio del transporte a través de las membranas celulares por difusión simple, es necesario considerar las leyes que rigen los procesos de difusión: las Leyes de Fick. Cuando un sistema presenta una diferencia en el número de moléculas por unidad de volumen (concentración), dentro y fuera de la membrana, se presenta un gradiente de concentración que es proporcional al número de partículas que atraviesan en la unidad de tiempo, un área unitaria perpendicular a la dirección de difusión, donde la constante de proporcionalidad esta dada por el coeficiente de difusión de las moléculas que atraviesan la membrana.
donde J es la densidad de corriente de partículas, D es el coeficiente de difusión y Al considerar una membrana de espesor, en la cual se presenta una diferencia de concentración ΔC = C2 − C1 constante, la primera Ley de Fick se puede reescribir como: El coeficiente de permeabilidad de la membrana es: La ecuación que expresa la conservación del número de moléculas, obtenida a partir del análisis del flujo entrante y saliente de las moléculas a través de un área y de la rapidez de acumulación (aumento por unidad de tiempo del número de partículas por unidad de volumen) es: Reemplazando, se obtiene: Segunda ley de Fick (ecuación de difusión)Con el objetivo de estudiar el comportamiento de las moléculas y de las variables que intervienen en el proceso de difusión, como lo son el gradiente de concentración y la densidad de flujo, se supone un modelo de membrana con espesor constante, a través de la cual solo se pueden transportar los gases O2,H2,CO2 con coeficientes de difusión y radios moleculares conocidos. En primer lugar, se ha supuesto que el gradiente de concentración varía de manera constante. A partir de ello y de la primera Ley de Fick, se halla la densidad de corriente de partículas J en función del gradiente de concentración DeltaC que permite hacer un análisis de la dependencia mutua de estas dos variables. Para obtener la solución a la segunda Ley de Fick, se supone que T < 0,C = 0 en todo el sistema considerado y que en t = 0 se introduce instantáneamente en el plano que corresponde a x = 0 una cantidad de sustancia igual a N moleculas/m2 (cuando el tiempo tiende a cero, la concentración también tiende a cero en todas partes excepto en x=0). Bajo estas condiciones la segunda Ley de Fick también debe satisfacer la condición de borde la solución de la segunda ley de Fick para una sola dimensión. ConclusionesEn el proceso de difusión simple con un gradiente de concentración constante, la densidad de flujo de partículas es directamente proporcional al gradiente de concentración. El corte con el eje y es cero, puesto que cuando no hay un gradiente de concentración, no se presenta flujo de partículas en ninguna dirección y por tanto el flujo neto es cero. Además, la pendiente de la recta representa la constante de proporcionalidad y corresponde al valor del coeficiente de difusión, por lo tanto, se puede ver que a mayor inclinación de la recta, mayor es el coeficiente de difusión. De acuerdo con la figura 2, la concentración relativa en función de las distancia recorrida por las moléculas, describe una distribución normal o gaussiana, en la que se puede ver que a menor tiempo de observación, la curva alcanza un valor máximo en su pico que representa el valor máximo de concentración relativa para cada tiempo, este pico se observa para
Bibliografía[1] Escobar Luis. Revista Actualidades Biológicas. Vol. 1 No. 2. Universidad de Antioquia, 1972; 42-46.
Categoría: Biología celular |
|
| Este articulo se basa en el articulo Difusión_simple_a_través_de_la_membrana_celular publicado en la enciclopedia libre de Wikipedia. El contenido está disponible bajo los términos de la Licencia de GNU Free Documentation License. Véase también en Wikipedia para obtener una lista de autores. |





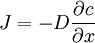 (1) Primera Ley de Fick.
(1) Primera Ley de Fick.
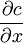 es el gradiente de concentración.
es el gradiente de concentración.
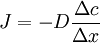
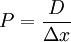
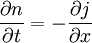
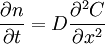
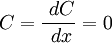 para
para 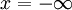 y
y 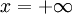 siendo la expresión final, obtenida a través de las transformadas de Fourier, siendo la expresión final:
siendo la expresión final, obtenida a través de las transformadas de Fourier, siendo la expresión final: