|
Disociación en química y bioquímica es un proceso general en el cual complejos, moléculas o sales se separan en moléculas más pequeñas, iones o radicales, usualmente de manera reversible. Disociación es lo opuesto de la asociación y de la recombinación. Producto destacado
Constante de disociaciónPara disociaciones reversibles en equilibrio químico. La constante de disociación Kc es la relación del componente disociado con respecto del asociado. SalesLa disociación en sales por solvatación en un solvente como agua significa la separación de los aniones y cationes. La sal puede recuperarse por la evaporación del solvente o por cristalización al reducir la temperatura. ÁcidosLa disociación de los ácidos en una solución significa la liberación de un protón H+, éste es un proceso de equilibrio, esto quiere decir que disociación y la recombinación ocurren al mismo tiempo con la misma velocidad. La constante de disociación de los ácidos Ka indica qué tan fuerte es un ácido, los ácidos fuertes poseen una Ka de mayor valor (por lo tanto menor pKa). El estudio de estos equilibrios se llama Equilibrio ácido-base. FragmentaciónLa fragmentación de una molécula puede darse por heterólisis u homólisis. PolímerosLos polímeros que son capaces de disociarse deben ser solubles en un determinado solvente, generalmente agua, allí pueden separse en iones, donde generalmente se forman polielectrolitos como los ácidos nucleicos (natural) o poli(ácido acrílico) o el Poli(ácido metacrílico) (sintéticos). El conocimiento sobre los polielectrolitos es el menor debido a su compleja química. Disociación del aguaLas propiedades de las disoluciones dependen del equilibrio del solvente, las disoluciones acuosas dependen del equilibrio de la disociación del agua. El agua, tanto en el estado puro como en el estado de disolvente es disociada en iones llamados hidrónio: H+ e hidroxilo: OH- Donde ac significa acuoso. Esta disociación, en dirección a la derecha ocurre únicamente hasta que el equilibrio se alcanza, después ocurre en ambas direcciones a la misma velocidad. Aproximadamente 1 de cada 500.000.000 de moléculas de agua se disocia. La ecuación se puede escribir igual que la de cualquier disociación: Siendo Kc la constante de disociación del agua, debido a que la disociación es prácticamente siempre la misma, se puede combinar con una nueva constante Kw: La constante kw no es de 1E14 sino de 1E(-14) Véase tambiénReferencias
Categoría: Procesos químicos |
|
| Este articulo se basa en el articulo Disociación publicado en la enciclopedia libre de Wikipedia. El contenido está disponible bajo los términos de la Licencia de GNU Free Documentation License. Véase también en Wikipedia para obtener una lista de autores. |





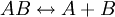
![K_c = \frac{([A] \cdot [B])}{[AB]}](images/math/e/b/e/ebe1ef5bee435b497b7e5e41c068c429.png)
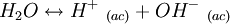
![K_c = \frac{([H^+] \cdot [OH^-])}{[H_{2}O]}](images/math/c/d/c/cdc132a9d93d7e2fd1494a9e54ef705f.png)
![K_c \cdot [H_{2}O] = K_w = [H^+] \cdot [OH^-] = 1,0\cdot10^{-14}](images/math/c/d/3/cd3dc45ddba32a8aba76e953dfd24b42.png)


