|
La adsorción es un proceso por el cual átomos, iones o moléculas son atrapadas o retenidas en la superficie de un material, en contraposición a la absorción, que es un fenómeno de volumen. En química, la adsorción de una sustancia es su acumulación en una determinada superficie interfacial entre dos fases. El resultado es la formación de una película líquida o gaseosa en la superficie de un cuerpo sólido o líquido. Considérese una superficie limpia expuesta a una atmósfera gaseosa. En el interior del material, todos los enlaces químicos (ya sean iónicos, covalentes o metálicos) de los átomos constituyentes están satisfechos. En cambio, por definición la superficie representa una discontinuidad de esos enlaces. Para esos enlaces incompletos, es energéticamente favorable el reaccionar con lo que se encuentre disponible, y por ello se produce de forma espontánea. La naturaleza exacta del enlace depende de las particularidades de los especímenes implicados, pero el material adsorbido es generalmente clasificado como fisisorbido o quimisorbido. La cantidad de material que se acumula depende del equilibrio dinámico que se alcanza entre la tasa a la cual el material se adsorbe a la superficie y la tasa a la cual se evapora, y que normalmente dependen de forma importante de la temperatura. Cuanto mayor sea la tasa de adsorción y menor la de desorción, mayor será la fracción de la superficie disponible que será cubierta por material adsorbido en el equilibrio. Para estos procesos, resultan interesantes materiales con una gran superficie interna, (y por lo tanto poco volumen) ya sea en polvo o granular, como el carbón activo, y llevan asociados otros fenómenos de transporte de material, como el macro transporte y micro transporte de los reactantes. Producto destacado
Termodinámica de la adsorción[1]La adsorción es el proceso mediante el cual un sólido poroso (a nivel microscópico) es capaz de retener partículas de gas en su superficie tras entrar en contacto con éste.
El adsorbente dispone de nanoporos, lo que se conoce como centros activos, en los que las fuerzas de enlace entre los átomos no están saturadas. Estos centros activos admiten que se instalen moléculas de naturaleza distinta a la suya, procedentes de un gas en contacto con su superficie. La adsorción es un proceso exotérmico y se produce por tanto de manera espontánea si el adsorbente no se encuentra saturado. La aplicación más importante de la termodinámica de la adsorción es la de calcular los equilibrios de fase entre un sólido adsorbente y una mezcla gaseosa. En este desarrollo, por simplicidad, sólo tomaremos en consideración gases puros (monocomponentes). La base de todo este cálculo son las isotermas de adsorción, las cuales dan la cantidad de gas adsorbido en los nanoporos como una función de la presión externa (del gas). La termodinámica sólo puede aplicarse a las isotermas de adsorción en el equilibrio. Esto significa que se debe poder llegar a cualquier punto de la curva elevando o disminuyendo la presión; en otras palabras, las curvas de adsorción y desadsorción tienen que coincidir. Esto ocurre sólo si no existe histéresis. La histéresis no se da en poros menores de 2 nm, sin embargo, se observa en poros lo suficientemente grandes como para que en su internior se condense gas para formar líquido. La isoterma de adsorción para un gas puro es la relación entre la cantidad adsorbida específica n (moles de gas por kilogramo de sólido) y P, la presión exterior de la fase gaseosa. La mayor parte de isotermas se pueden ajustar mediante una ecuación del virial modificada: ![P(n)=\frac{n}{K}\left[\frac{m}{m-n}\right]e^{[C_1n+C_2n^2+C_3n^3+...]} \qquad para \qquad n<m \qquad (1)](images/math/8/6/8/8680bc0b162f9921d96f8864277a64b4.png) donde K es la constante de Henry (el valor de la isoterma de adsorción dn/dP cuando la presión tiende a cero), m la capacidad de saturación del medio sólido (mol kg-1) y Ci son los coeficientes del virial. Normalmente tres coeficientes bastan para ajustar la curva a los datos experimentales.
Nótese que las isotermas han de obtenerse a partir de la interpolación de datos experimentales, aunque existen también modelos moleculares, al margen de la termodinámica, de los que se pueden obtener teóricamente las propiedades del sistema. La interpolación de las isotermas de adsorción respecto de la temperatura se basa en la ecuación ![\bar h = R \left[ \frac{\partial \ln P}{\partial (1/T)} \right]_n \qquad (2)](images/math/5/f/0/5f02f9712f7f13636f26cd1a52c86bf2.png) donde Normalmente la entalpía diferencial se calcula a partir de la ecuación (2) haciendo uso de dos o más isotermas de adsorción. El gran potencial juega un papel fundamental en la termodinámica de la adsorción. Se define como 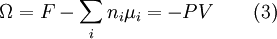 donde F es la energía libre de Helmholtz. Las variables independientes son temperatura, volumen y potencial químico. Para adsorción en un gas puro, el gran potencial se obtiene a partir de la integración de una isoterma: ![\Omega = - RT \int_0^R \frac{n}{P} dP = - RT \int_0^n \left[ \frac{\partial ln P}{\partial n} \right]_T dn \qquad (4)](images/math/4/6/0/460c28d0717641507645916acbf6883c.png) Ω se expresa en J kg-1 de adsorbente sólido. El significado físico del gran potencial es la variación de energía libre asociada a la inmersión isotérmica del adsorbente 'virgen' en el volumen del gas. La entalpía de inmersión H es la integral de la entalpía diferencial: 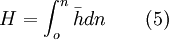 Al igual que Ω, tiene unidades de J kg-1. Una vez obtenidas la energía de inmersión (Ω) y la entalpía de inmersión (H), la entropía de inmersión es: 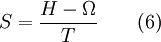 A partir de estas ecuaciones se puede hacer todo el análisis termodinámico en un sistema formado por un adsorbente y un gas. No debemos dejar de tener en cuenta que la determinación de la ecuación (1), de donde hemos derivado todas las demás, se hace a partir de mediciones experimentales. FisisorciónLa fisisorción es la forma más simple de adsorción, y es debida a débiles fuerzas atractivas, generalmente fuerzas de Van der Waals (véase fuerzas dispersivas). Dado que estas fuerzas son omnipresentes, resulta que rápidamente cualquier superficie limpia expuesta al ambiente acumula una capa de material fisisorbido. QuimisorciónLa quimisorción ocurre cuando un enlace químico, definido en este caso como un intercambio de electrones, se forma. El grado de intercambio y lo simétrico que sea dependen de los materiales involucrados. A menudo hay un paralelismo con las situaciones encontradas en química de coordinación. La quimisorción es particularmente importante en la catálisis heterogénea, la forma más común en la industria, donde un catalizador sólido interacciona con un flujo gaseoso, el reactante o los reactantes, en lo que se denomina reacción en lecho fluido. La adsorción del reactante por la superficie del catalizador crea un enlace químico, alterando la densidad electrónica alrededor de la molécula reactante y permitiendo reacciones que normalmente no se producirían en otras circunstancias. La corrosión es un ejemplo de ello.
AplicacionesUna de las aplicaciones más conocidas de la adsorción en el mundo industrial, es la extracción de humedad del aire comprimido. Se consigue haciendo pasar el aire comprimido a través de un lecho de alumina activa u otros materiales con efecto de adsorción a la molécula de agua. La saturación del lecho se consigue sometiendo a presión el gas o aire, así la molécula de aire es adsorbida por la molécula del lecho, hasta su saturación. La regeneración del lecho, se consigue soltando al exterior este aire comprimido y haciendo pasar una corriente de aire presecado a traves del lecho. Lo habitual es encontrar secadores de adsorción en forma de dos columnas y mientras una adsorbe, la otra es regenerada por el mismo aire seco de la columna anterior. Este sistema se conoce como "pressure spring" o PSA. Véase también
Referencias
|
|
| Este articulo se basa en el articulo Adsorción publicado en la enciclopedia libre de Wikipedia. El contenido está disponible bajo los términos de la Licencia de GNU Free Documentation License. Véase también en Wikipedia para obtener una lista de autores. |





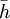 es la entalpía de adsorción diferencial, negativa porque la adsorción es un proceso exotérmico, como ya hemos comentado. El valor absoluto de
es la entalpía de adsorción diferencial, negativa porque la adsorción es un proceso exotérmico, como ya hemos comentado. El valor absoluto de 

