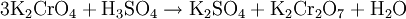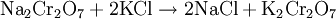El dicromato de potasio (K2Cr2O7) es una sal del hipotético ácido dicrómico (este ácido en sustancia no es estable) H2Cr2O7. Se trata de una sustancia de color intenso anaranjado. Es un oxidante fuerte. En contacto con sustancias orgánicas puede provocar incendios. Producto destacado
SíntesisEl dicromato potásico se obtiene a partir del cromato potásico acidulando la disolución correspondiente:
También se puede obtener por intercambio del catión a partir del dicromato de sodio y cloruro de potasio:
ReaccionesEsta reacción se utiliza a veces para la determinación cualitativa del cromo(VI). En presencia de iones de bario o de plomo(II) en disolución neutra o ligeramente ácida precipitan los cromatos correspondientes en forma de sólidos amarillos. Ambos se disuelven en ácidos fuertes, el cromato de plomo también en presencia de base fuerte. Estas sustancias se utilizan como pigmentos en algunas pinturas amarillas. En disolución ácida y presencia de cloruro se forma el anión ClCrO4- que puede cristalizar en forma de su sal potásica. Calentándolo con ácido clorhídrico concentrado se forma cloruro de cromil (Cl2CrO4), una sustancia anaranjada molecular que puede ser destilada de la mezcla de reacción. ¡CUIDADO! EL CLORURO DE CROMIL SE PUEDE DESCOMPONER DE FORMA EXPLOSIVA. AplicacionesEl dicromato de potasio se utiliza en la galvanotécnica para cromar otros metales, en la fabricación del cuero, en la fabricación de pigmentos, como reactivo en la industria química, para recubrimientos anticorrosivos del cinc y del magnesio y en algunos preparados de protección de madera. También está presente en los antiguos tubos de alcotest donde oxida el etanol del aire expirado al aldehído. En química analítica se utiliza para determinar la demanda química de oxígeno (DQO) en muestras de agua. Históricamente importante es la reacción del dicromato potásico con anilina impura que utilizó W.H.Perkin en la síntesis de la mauveina, el primer colorante artificial. Esta reacción era una de las primeras síntesis orgánicas industriales. ToxicologíaEl dicromato de potasio es tóxico. En contacto con la piel se produce sensibilización y se pueden provocar alergias. Al igual que los cromatos los dicromatos son cancerígenos. En el cuerpo son confundidos por los canales iónicos con el sulfato y pueden llegar así hasta el núcleo de la célula. Allí son reducidos por la materia orgánica presente y el cromo(III) formado ataca a la molécula de la ADN. Residuos que contienen dicromato de potasio se pueden tratar con sulfato de hierro(II)(FeSO4). Este reduce el cromo(VI) a cromo(III) que precipita en forma del hidróxido o del óxido Referencias externas
|
|||||||||||||||||||||||||||||||||||||||||||||
| Este articulo se basa en el articulo Dicromato_de_potasio publicado en la enciclopedia libre de Wikipedia. El contenido está disponible bajo los términos de la Licencia de GNU Free Documentation License. Véase también en Wikipedia para obtener una lista de autores. | |||||||||||||||||||||||||||||||||||||||||||||

Último visto