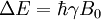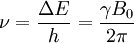|
La resonancia magnética o RM (también conocida como resonancia magnética nuclear o RMN) es un fenómeno físico basado en las propiedades magnéticas que poseen los núcleos atómicos. La RM permite alinear los campos magnéticos de diferentes núcleos en la dirección de un campo magnético externo. La respuesta a este campo externo depende del tipo de núcleos atómicos, por lo que esta técnica puede utilizarse para obtener información sobre una muestra. Conocimientos adicionales recomendados
Aplicaciones más comunesLa resonancia magnética hace uso de las propiedades de resonancia aplicando radiofrecuencias a los átomos o dipolos entre los campos alineados de la muestra, y permite estudiar la información estructural o química de una muestra. La RM se utiliza también en el campo de la investigación de ordenadores cuánticos. Sus aplicaciones más frecuentes se encuentran ligadas al campo de la medicina, la bioquímica y la química orgánica. Es común denominar "resonancia magnética" al aparato que obtiene imágenes por resonancia magnética (MRI, por las siglas en inglés de "Magnetic Resonance Imaging"). Principio físicoTodos los núcleos que contienen un número impar de protones (número atómico) o un número másico impar tienen un momento magnético intrínseco y un momento angular. Si un núcleo con estas características se somete a un campo magnético constante, percibirá un par de fuerzas que lo harán girar sobre sí mismo hasta que el momento magnético y el campo magnético se encuentren alineados. Dos alineamientos serán posibles. Por una parte, el campo magnético y el momento magnético pueden apuntar en la misma dirección, configuración que tendrá una energía mínima y será la más probable. Por la otra, ambos vectores pueden apuntar en direcciones opuestas, caso en el que la energía será ligeramente superior. La diferencia de energía entre ambos estados se expresa según la ecuación siguiente: Donde γ es la constante giromagnética o factor giromagnético, que depende del núcleo que observemos. Ambos niveles estarán poblados según las leyes del equilibrio térmico. Como se puede observar, la diferencia de energía es proporcional a la magnitud del campo magnético y está directamente relacionada con la frecuencia de Larmor. Podemos expresar la diferencia de energía en forma de la frecuencia del campo electromagnético cuyos fotones tienen esta energía. Debido a esta diferencia de energía, si un núcleo es perturbado por un campo electromagnético de la frecuencia apropiada, se producirá un fenómeno de resonancia; los núcleos del estado de energía inferior se excitarán al estado de energía superior. Cuando el estímulo cese, los núcleos emitirán, en forma de fotones, la energía que habían absorbido. Fotones que podrán detectarse utilizando el equipamiento adecuado. Las frecuencias necesarias para producir el fenómeno de resonancia se encuentran dentro del rango de la radiofrecuencia. El núcleo más utilizado para observar el efecto son: el protio (1H), por ser el más abundante y fácil de encontrar, y el carbono-13 (13C). Otros isótopos que pueden utilizarse son: 15N, 14N, 19F, 31P, 17O, 29Si, 10B, 11B, 23Na, 35Cl y 195Pt. Los equipos médicos de resonancia magnética nuclear suelen trabajar a una frecuencia de 300 MHz para la resonancia de H1, y entre 20 MHz y 50 MHz para otros átomos. Referencias
Enlaces externos
Véase también
|
|
| Este articulo se basa en el articulo Resonancia_magnética publicado en la enciclopedia libre de Wikipedia. El contenido está disponible bajo los términos de la Licencia de GNU Free Documentation License. Véase también en Wikipedia para obtener una lista de autores. |


Enciclopedia