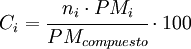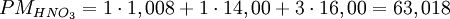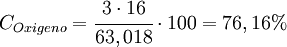|
La composición centesimal indica el porcentaje, en masa, de cada elemento que forma parte de un compuesto. Se obtiene a partir de la fórmula molecular del compuesto, ya que ésta nos indica el número de átomos de cada elemento presentes en el compuesto. Producto destacadoPara calcular la composición centesimal de cada elemento, se aplica la siguiente expresión: En donde ni indica el número de átomos del elemento i considerado y PMi la masa atómica de dicho elemento. El denominador es la masa molecular del compuesto. EjemploQueremos calcular el porcentaje de oxígeno presente en el ácido nítrico. Las masas moleculares son:
La fórmula del ácido nítrico es HNO3, así sabemos que una molécula de ácido nítrico contiene un átomo de hidrógeno, uno de nitrógeno y tres de oxígeno. Aplicamos la fórmula anterior para el oxígeno. Lo mismo puede repetirse para cada elemento. Esta fórmula es válida para compuestos moleculares; se puede aplicar igualmente si tratamos con compuestos iónicos, tomando como peso molecular de dicho compuesto al correspondiente a una celda unidad; en el caso de un cristal de cloruro de sodio (NaCl, sal común), la fórmula molecular que tomaríamos sería NaCl. Esta fórmula no puede aplicarse a compuestos no estequiométricos o aleaciones, ya que estas últimas se consideran una mezcla de elementos y no un compuesto químico, y los primeros tienen una "fórmula" variable. Referencias
Categoría: Propiedades químicas |
| Este articulo se basa en el articulo Composición_centesimal publicado en la enciclopedia libre de Wikipedia. El contenido está disponible bajo los términos de la Licencia de GNU Free Documentation License. Véase también en Wikipedia para obtener una lista de autores. |