Los químicos crean una nueva enzima artificial
La molécula de triple cadena puede ayudar a poner el santo grial de la química al alcance
Anuncios
Las enzimas son los motores de la naturaleza. Se encuentran en las células de todos los animales, plantas y todos los demás organismos vivos, y aceleran las reacciones químicas que desencadenan miles de funciones biológicas, desde la formación de neuronas hasta la digestión de los alimentos.

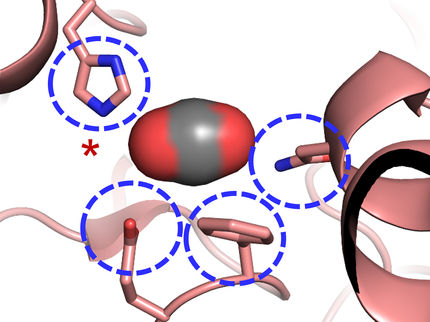
Utilizando la química computacional, el estudiante de postgrado Vindi M. Jayasinghe-Arachchige y Rajeev Prabhakar, profesor de química, diseñaron una nueva molécula que podría avanzar significativamente en el estudio y los usos de las enzimas.
Jenny Hudak/University of Miami
Realizan su trabajo de forma tan selectiva y tan rápida -millones de veces más rápido que un parpadeo- que el campo de la química biomimética ha surgido en las últimas décadas con el objetivo de diseñar enzimas artificiales que puedan imitar los poderes de las enzimas naturales en entornos industriales. Las enzimas artificiales podrían, por ejemplo, convertir el maíz en etanol o ayudar a crear nuevos medicamentos de forma más rápida, barata y eficaz.
Acercándose un paso más a la consecución de ese objetivo, Rajeev Prabhakar, un químico computacional de la Universidad de Miami, y sus colaboradores de la Universidad de Michigan han creado una novedosa molécula sintética de tres hebras que funciona igual que una metaloenzima natural, o una enzima que contiene iones metálicos.
"No estaba claro que se pudieran hacer, pero las hicimos. Y luego las usamos para catalizar con éxito las reacciones", dijo Prabhakar, un profesor de química que estudia las reacciones enzimáticas con la esperanza de diseñar sus análogos artificiales. "Este es un paso incremental pero importante en el desarrollo de enzimas artificiales, que durante mucho tiempo se ha considerado el santo grial de la química. Desafortunadamente, tan bien como las enzimas naturales trabajan en nuestros cuerpos y otras formas de vida, no toleran muy bien otros entornos. También son muy caras y no son fáciles de preparar y purificar".
Para su innovador estudio publicado en Nature Chemistry, Prabhakar y el estudiante de postgrado Vindi M. Jayasinghe-Arachchige se unieron a Vincent L. Pecoraro, un profesor de química de la Universidad de Michigan, para mejorar el rendimiento de las enzimas artificiales de las que el laboratorio de Pecoraro fue pionero a lo largo de los años. Los investigadores de Michigan habían creado previamente metalloenzimas sintéticas más simples que catalizaron con éxito una serie de reacciones químicas. Pero esas macromoléculas artificiales fueron diseñadas con tres cadenas homotriméricas idénticas o simétricas, lo que, según Prabhakar, limitó sus capacidades catalíticas.
En la nueva molécula, que Jayasinghe-Arachchige diseñó en la supercomputadora de la Universidad de Miami con la guía de Prabhakar, la tercera hebra difiere en estructura de las otras dos hebras. Sus cálculos de mecánica cuántica mostraron que la estructura más compleja, no simétrica, de tres hebras, conocida como bobina "heterotrimérica", expandió el rendimiento catalítico de las metalo-enzimas artificiales homotriméricas, un hallazgo que Pecoraro y su equipo confirmaron con experimentos en su laboratorio de Michigan.
"Nuestras técnicas son diferentes, pero complementarias", dijo Prabhakar. "Lo que hacemos el grupo Pecoraro no puede hacerlo, y lo que ellos hacen, nosotros no podemos hacerlo. Modelamos las moléculas en el ordenador para poder predecir sus propiedades estructurales y el mecanismo de sus formaciones. Usan nuestros modelos para construir la cosa real, y en este caso es el primer ejemplo de una molécula heterotrimérica natural".
La mayoría de los legos probablemente encontraría el estudio tan incomprensible como su título: "Bobinas heterotriméricas de tres hebras diseñadas usando una estrategia mediada por una plantilla de Pb(II)(Cys)3". Pero el resultado final, dijo Prabhakar, es que la investigación colaborativa llevada a cabo en Miami y Michigan abre la puerta a una nueva estrategia para lograr la creación de enzimas artificiales que funcionen tan bien como las enzimas naturales.
Además de Pecocaro, Prabhakar y Jayasinghe-Arachchige, otros coautores del estudio son el antiguo estudiante de posgrado de Prabhakar, Thomas J. Paul, actualmente en la Universidad de Michigan; Audrey E. Tolbert, Catherine S. Ervin y Kosh P. Neupane, también de la Universidad de Michigan; y Leela Ruckthong, de la Universidad Tecnológica del Rey Mongkut, en Tailandia.
Ahora en su último año de estudio para su doctorado en química, Jayasinghe-Arachchige dijo que sigue fascinada por los avances en las técnicas de química computacional que le permitieron modelar las estructuras químicas y las reacciones de la nueva molécula.
"Estoy entusiasmada de que nuestros hallazgos creen nuevas vías para el desarrollo de enzimas artificiales eficientes que puedan ser utilizadas para mejorar la calidad de vida", dijo Jayasinghe-Arachchige, "y como mujer en un campo donde las mujeres están subrepresentadas, espero que este estudio motive a las mujeres a unirse al fascinante mundo de los campos STEM".
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.