El nuevo procedimiento reducirá la necesidad de metales raros en la síntesis química
Los investigadores están trabajando para mejorar la sostenibilidad a largo plazo de las síntesis farmacéuticas y otras síntesis químicas
Anuncios
Los productos farmacéuticos, plásticos y muchos otros productos químicos han transformado la vida humana. Para preparar estos productos, los químicos a menudo usan un catalizador - frecuentemente basado en metales raros - en varios puntos de sus síntesis. Aunque los catalizadores de metales raros son increíblemente útiles, su suministro limitado significa que su uso es insostenible a largo plazo. Los químicos sintéticos necesitan una alternativa.
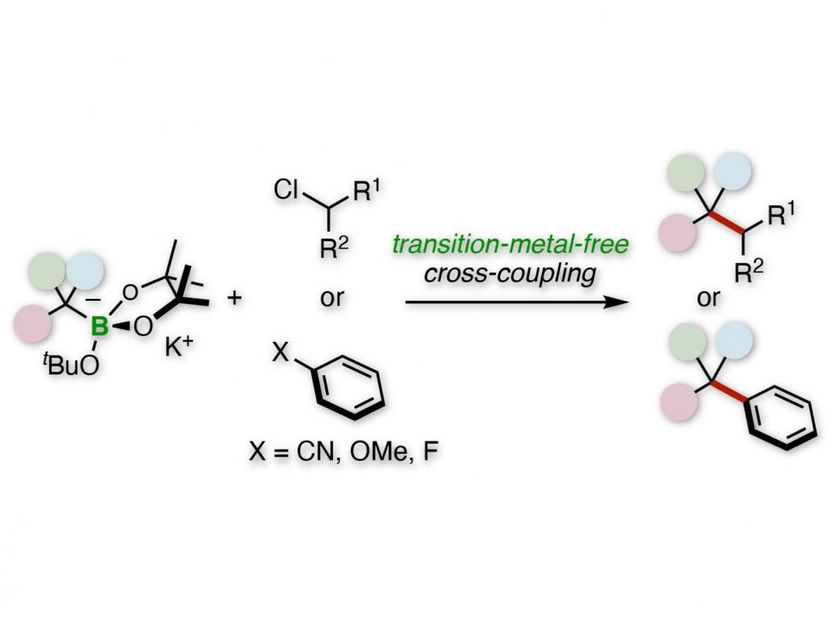
Acoplamiento cruzado de electrofilos de alquilo o arilo en el terciario.
Kanazawa University
En un estudio recientemente publicado en Angewandte Chemie, los investigadores de la Universidad de Kanazawa informan de tal alternativa. Su investigación sobre una amplia clase de reacciones químicas que son comunes en las síntesis farmacéuticas y de otro tipo preparará el camino para una industria química más sostenible.
El Premio Nobel de Química de 2010 fue para los investigadores que utilizaron catalizadores basados en paladio metálico para realizar un tipo de reacción química común conocida como acoplamiento cruzado. Tales catalizadores funcionan muy bien para sintetizar lo que se conoce como centros de carbono cuaternario congestionado, que son comunes en las moléculas utilizadas en la agricultura y la medicina. Sin embargo, para la sostenibilidad a largo plazo, los investigadores necesitan una alternativa a los catalizadores de metales raros.
"Utilizamos organoboratos bencílicos para realizar el acoplamiento cruzado alquilante terciario de los electrofilos arilo o alquilo", dice Hirohisa Ohmiya, autor correspondiente del estudio. "Nuestro procedimiento no utiliza elementos raros y es una ruta directa a los centros de carbono cuaternario".
Los estudios iniciales de los investigadores consistieron en un bencilboronato terciario que se activa primero por una base de alcóxido de potasio para convertirse en un anión bencílico. Este anión se somete entonces a una reacción de acoplamiento cruzado con un electrofilo de cloruro de alquilo secundario.
"La reacción tiene un amplio alcance", explica el autor correspondiente Hirohisa Ohmiya. "Por ejemplo, la sustitución del grupo fenilo del boronato por varios anillos aromáticos tuvo éxito, y el electrófilo puede ser una amplia gama de anillos y cadenas lineales".
Estudios posteriores reemplazaron el cloruro de alquilo secundario con varios nitrilos arilo, éteres arilo y fluoruros arilo. Muchas de estas reacciones tuvieron éxito, como las de la 4-cianopiridina y el 4-fluorofenilbenceno.
Un comentario en Nature el 19 de noviembre indica que la pandemia de COVID-19 ha interrumpido las cadenas de suministro de varios metales raros que son pertinentes para la industria química. Cientos de minas y fábricas han sido cerradas, y muchas fronteras nacionales están más restringidas que antes de la pandemia. Una solución a largo plazo para las interrupciones de la cadena de suministro es desarrollar protocolos sintéticos que no utilicen metales raros. La investigación descrita aquí es una parte importante de ese esfuerzo y ayudará a que las síntesis químicas sean más sostenibles para las generaciones futuras.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.











































