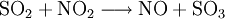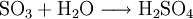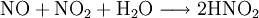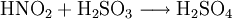El ácido sulfúrico es un compuesto químico muy corrosivo cuya fórmula es H2SO4. Es el compuesto químico que más se produce en el mundo, por eso se utiliza como uno de los tantos medidores de la capacidad industrial de los países. Una gran parte se emplea en la obtención de fertilizantes. También se usa para la síntesis de otros ácidos y sulfatos y en la industria petroquímica. Generalmente se obtiene a partir de dióxido de azufre, por oxidación con óxidos de nitrógeno en disolución acuosa. Normalmente después se llevan a cabo procesos para conseguir una mayor concentración del ácido. Antiguamente se lo denominaba aceite o espíritu de vitriolo, porque se producía a partir de este mineral. La molécula presenta una estructura piramidal, con el átomo de azufre en el centro y los cuatro átomos de oxígeno en los vértices. Los dos átomos de hidrógeno están unidos a los átomos de oxígeno no unidos por enlace doble al azufre. Dependiendo de la disolución, estos hidrógenos se pueden disociar. En agua se comporta como un ácido fuerte en su primera disociación, dando el anión hidrogenosulfato, y como un ácido débil en la segunda, dando el anión sulfato. Además reacciona violentamente con agua y compuestos orgánicos con desprendimiento de calor. Producto destacado
HistoriaEl descubrimiento del ácido sulfúrico se relaciona con el siglo VIII y el alquimista Jabir ibn Hayyan. Fue estudiado después, en el siglo IX por el alquimista Ibn Zakariya al-Razi, quien obtuvo la sustancia de la destilación seca de minerales incluyendo la mezcla de sulfato de hierro(II) (FeSO4) con agua y sulfato de cobre(II) (CuSO4). Calentados, estos compuestos se descomponen en óxido de hierro y oxido de cobre, respectivamente, dando agua y trióxido de azufre, que combinado produce una disolución diluida de ácido sulfúrico. Este método se hizo popular en Europa a través de la traducción de los tratados y libros de árabes y persas por alquimistas europeos del siglo XIII como el alemán Albertus Magnus. Los alquimistas de la Europa medieval conocían al ácido sulfúrico como aceite de vitriolo, licor de vitriolo, o simplemente vitriolo, entre otros nombres. La palabra vitriolo deriva del latín “vitreus”, que significa cristal y se refiere a la apariencia de las sales de sulfato, que también reciben el nombre de vitriolo. Las sales denominadas así incluyen el sulfato de cobre II (o ‘vitriolo azul’ o ‘vitriolo romano’), sulfato de zinc (o ‘vitriolo blanco’), sulfato de hierro II (o ‘vitriolo verde’), sulfato de hierro(III) (o ‘vitriolo de Marte’), y sulfato de cobalto II (o ‘vitriolo rojo’). El vitriolo era considerado la sustancia química más importante, y se intentó utilizar como piedra filosofal. Altamente purificado, el vitriolo se utilizaba como medio para hacer reaccionar sustancias en él. En el siglo XVII, el químico alemán-holandés Johann Glauber consiguió ácido sulfúrico quemando azufre con nitrato de potasio (KNO3), en presencia de vapor. A medida que el nitrato de potasio se descomponía, el azufre se oxidaba en SO3, que combinado con agua producía el ácido sulfúrico. En 1736, Joshua Ward, un farmacéutico londinense utilizó este método para empezar a producir ácido sulfúrico en grandes cantidades. En 1746 en Birmingham, John Roebuck empezó a producirlo de esta forma en cámaras de plomo, que eran más fuertes y resistentes y más baratas que las de cristal que se habían utilizado antes. Este proceso de cámara de plomo, permitió la efectiva industrialización de la producción de ácido sulfúrico, que con pequeñas mejoras mantuvo este método de producción durante al menos dos siglos. El ácido obtenido de esta forma, tenía una concentración de tan solo 35-40%. Mejoras posteriores, llevabas a cabo por el francés Joseph-Louis Gay-Lussac y el británico John Glover consiguieron aumentar esta cifra hasta el 78%. Sin embargo, la manufactura de algunos tintes y otros productos químicos que requerían en sus procesos una concentración mayor lo consiguieron en el siglo XVIII con la destilación en seco de minerales con una técnica similar a la de los alquimistas precursores. Quemando pirita (disulfuro de hierro) con sulfato de hierro a 480º conseguía ácido sulfúrico de cualquier concentración, pero este proceso era tremendamente caro y no era rentable para la producción industrial o a gran escala. En 1831, el vendedor de vinagre Peregrine Phillips patentó un proceso de conseguir trióxido de azufre y ácido sulfúrico concentrado mucho más económico, ahora conocido como el proceso de contacto. Actualmente, la mayor parte del suministro de ácido sulfúrico se obtiene por este método. Formación del ácidoEl ácido sulfúrico se encuentra disponible comercialmente en un gran número de concentraciones y grados de pureza. Existen dos procesos principales para la producción de ácido sulfúrico, el método de cámaras de plomo y el proceso de contacto. El proceso de cámaras de plomo es el más antiguo de los dos procesos y es utilizado actualmente para producir gran parte del acido consumido en la fabricación de fertilizantes. Este método produce un ácido relativamente diluido (62%-78% H2SO4). El proceso de contacto produce un ácido más puro y concentrado, pero requiere de materias primas más puras y el uso de catalizadores costosos. En ambos procesos el dióxido de azufre (SO2) es oxidado y disuelto en agua. El dióxido de azufre es obtenido mediante la incineración azufre, tostando piritas (Disulfuro de hierro), tostando otros sulfuros no ferrosos, o mediante la combustión de sulfuro de hidrógeno (H2S) gaseoso. Proceso de cámaras de plomoEn el proceso de cámaras de plomo dióxido de azufre (SO2) gaseoso caliente entra por la parte inferior de un reactor llamado torre de Glover donde es lavado con vitriolo nitroso (ácido sulfúrico con óxido nítrico (NO) y dióxido de nitrógeno (NO2) disueltos en él), y mezclado con oxido de nitrógeno (NO) y dióxido de nitrógeno (NO2) gaseosos. Parte de dióxido de azufre es oxidado a trióxido de azufre (SO3) y disuelto en el baño ácido para formar el ácido de torre o ácido de Glover (aproximadamente 78% de H2SO4). De la torre de Glover una mezcla de gases (que incluye dióxido y tritóxido de azufre, óxidos de nitrógeno, nitrógeno, oxigeno y vapor) es transferida a una cámara recubierta de plomo donde es tratado con más agua. La cámara puede ser un gran espacio en forma de caja o un recinto con forma de cono truncado. El ácido sulfúrico es formado por una serie compleja de reacciones; condensa en las paredes y es acumulado en el piso del la cámara. Pueden existir de tres a seis cámaras en serie, donde los gases pasan por cada una de las cámaras en sucesión. El ácido producido en las cámaras, generalmente llamado ácido de cámara o ácido de fertilizante, contiene de 62% a 68% de H2SO4. Luego de que los gases pasaron por las cámaras se los hace pasar a un reactor llamado torre de Gay-Lussac donde son lavados con ácido concentrado enfriado (proveniente de la torre de Glover). Los óxidos de nitrógeno y el dióxido de azufre que no haya reaccionado se disuelven en el ácido formando el vitriolo nitroso utilizado en la torre de Glover. Los gases remanentes son usualmente liberados en la atmósfera. Proceso de contactoEl proceso se basa en el empleo de un catalizador para convertir el SO2 en SO3, del que se obtiene ácido sulfúrico por hidratación. En este proceso, una mezcla de gases secos que contiene del 7 al 10% de SO2, según la fuente de producción de SO2 (el valor inferior corresponde a plantas que tuestan piritas y el superior a las que queman azufre), y de un 11 a 14% de O2, se precalienta y una vez depurada al máximo, pasa a un convertidor de uno o más lechos catalíticos, por regla general de platino o óxido de vanadio (V), donde se forma el SO3. Se suelen emplear dos o más convertidores. Los rendimientos de conversión del SO2 a SO3 en una planta en funcionamiento normal oscilan entre el 96 y 97%, pues la eficacia inicial del 98% se reduce con el paso del tiempo. Este efecto de reducciones se ve más acusado en las plantas donde se utilizan piritas de partida con un alto contenido de arsénico, que no se elimina totalmente y acompaña a los gases que se someten a catálisis, provocando el envenenamiento del catalizador. Por consiguiente, en ocasiones, el rendimiento puede descender hasta alcanzar valores próximos al 95%. En el segundo convertidor, la temperatura varia entre 500º y 600°C. Esta se selecciona para obtener una constante óptima de equilibrio con una conversión máxima a un coste mínimo. El tiempo de residencia de los gases en el convertidor es aproximadamente de 2-4 segundos. Los gases procedentes de la catálisis se enfrían a unos 100°C aproximadamente y atraviesan una torre de óleum, para lograr la absorción parcial de SO3. Los gases residuales atraviesan una segunda torre, donde el SO3 restante se lava con ácido sulfúrico de 98%. Por ultimo, los gases no absorbidos se descargan a la atmósfera a través de una chimenea. Existe una marcada diferencia entre la fabricación del SO2 por combustión del azufre y por tostación de piritas, sobre todo si son arsenicales. El polvo producido en el proceso de tostación nunca puede eliminarse en su totalidad y, junto con las impurezas, principalmente arsénico y antimonio, influye sensiblemente sobre el rendimiento general de la planta. La producción de el ácido sulfúrico por combustión de azufre elemental presenta un mejor balance energético pues no tiene que ajustarse a los sistemas de depuración tan rígidos forzosamente necesarios en las plantas de tostación de piritas. Otras aplicacionesAdemás de las mencionadas, también se lo emplea para:
CuriosidadesLa preparación de una disolución de ácido puede resultar peligrosa por el calor generado en el proceso. Es vital que el ácido concentrado sea añadido al agua (y no al revés) para aprovechar la alta capacidad calorífica del agua. En caso de añadir agua al ácido concentrado, pueden producirse salpicaduras de ácido.[1] [2] ReferenciasVéase tambiénEnlaces externos
|
|||||||||||||||||||||||||||||||||||||||||||||
| Este articulo se basa en el articulo Ácido_sulfúrico publicado en la enciclopedia libre de Wikipedia. El contenido está disponible bajo los términos de la Licencia de GNU Free Documentation License. Véase también en Wikipedia para obtener una lista de autores. | |||||||||||||||||||||||||||||||||||||||||||||