|
El calor específico o más formalmente la capacidad calorífica específica de una sustancia es una magnitud física que indica la capacidad de un material para almacenar energía interna en forma de calor.[1] De manera formal es la energía necesaria para incrementar en una unidad de temperatura una cantidad de sustancia; usando el SI es la cantidad de joules de energía necesaria para elevar en un 1 K la temperatura de 1 kg de masa.[2] Se la representa por lo general con la letra c. Se necesita más energía calorífica para incrementar la temperatura de una sustancia con un alto valor del calor específico que otra con un valor pequeño. Por ejemplo, se requiere ocho veces más energía para incrementar la temperatura de un lingote de magnesio que para un lingote de plomo de la misma masa.[1] El calor específico es pues una propiedad intensiva, por lo que es representativa de cada sustancia, mientras que la capacidad calorífica, de la cual depende, es una propiedad extensiva y es representativa de cada cuerpo particular.[3] Matemáticamente el calor específico es la razón entre la capacidad calorífica de un objeto y su masa.[1] El término se originó por el trabajo del físico Joseph Black quien condujo varias medidas del calor y usó la frase “capacidad para el calor”,[4] en ese entonces la mecánica y la termodinámica se consideraban ciencias independientes, por lo que el término podría parecer inapropiado, tal vez un mejor nombre podría ser transferencia de calor específica, pero el término está demasiado arraigado para ser reemplazado.[5] Producto destacado
Definición y UnidadesEcuaciones BásicasEl calor específico se define de la siguiente forma: Donde Asimismo, para hallar el calor se puede dividir el incremento de temperatura en N intervalos pequeños ΔTn, si suponemos que cn es constante en los intervalos pequeños desde Ti hasta Tf entonces se sigue que: donde c es una función de la Temperatura del objeto. Esta función es creciente para la mayoría de las sustancias (excepto los gases monoatómicos y diatómicos). Esto se debe a efectos cuánticos que hacen que los modos de vibración estén cuantizados y sólo estén accesibles a medida que aumenta la temperatura. De manera diferencial esto resulta en: De una manera no diferencial O bien Cantidad de sustanciaCuando se mide el calor específico en ciencia e ingeniería, la cantidad de sustancia es a menudo de masa: ya sea en gramos o en kilogramos, ambos del SI. Especialmente en química, sin embargo, conviene que la unidad de la cantidad de sustancia sea el mol al medir el calor específico, el cual es un cierto número de de moléculas o átomos o de moléculas de la sustancia.[6] Cuando la unidad de la cantidad de sustancia es el mol, el término calor específico molar se puede usar para referirse de manera explícita a la medida; o bien usar el término calor específico másico, para indicar que se usa una unidad de masa. CalorLa unidad de medida del calor en el Sistema Internacional es el julio. La caloría también se usa a menudo en Química. Al usar calorías como unidad de medida del calor, es importante notar que la caloría esta definida como el calor necesario para aumentar en 1 °C la temperatura de un gramo de agua destilada,[7] es decir tiene una definición basada en el calor específico. Esto significa que al medir el calor específico (a presión constante) usando calorías, todas las sustancias con un calor específico menor que el del agua tendrán su medición con una magnitud menor que 1 y los que tengan un calor específico mayor la tendrán mayor que 1.[5] Intervalo de temperaturaEl intervalo de temperatura, en Física, Ingeniería y Química es por lo general el Kelvin, o el grado Celsius (ambos tienen la misma magnitud). Otras unidadesEn los Estados Unidos y en los otros países donde se sigue utilizando el Sistema Anglosajón de Unidades, el calor específico se suele medir en BTU (unidad de calor) por libra (unidad de masa) y grado Fahrenheit (unidad de temperatura). La BTU se define como la cantidad de calor que se requiere para elevar un grado Fahrenheit la temperatura de una libra de agua en condiciones atmosféricas normales.[8] Símbolos y estándaresEn Física e Ingeniería, es de uso corriente designar C mayúscula a la capacidad calorífica, y c minúscula al calor específico; en Química en cambio es más frecuente usar las mayúsculas para indicar que la unidad de la cantidad de sustancia es el mol y la minúscula para la masa. Las unidades del SI son los Joules por gramo-Kelvin (J g–1 K–1) o el Joule por mol-Kelvin (J mol–1 K–1). Se pueden crear, sin embargo, distintas variantes de estas unidades, como por ejemplo kJ kg–1 K–1 y kJ mol–1 K–1). Hay dos condiciones notablemente distintas bajo las que se mide el calor específico y estas se denotan con sufijos a la letra c. El calor específico de los gases normalmente se mide bajo condiciones de presión constante (Símbolo: cp). Las mediciones bajo presión constante producen valores mayores que aquellas bajo volumen constante, debido a que debe realizarse un trabajo para la primera. El cociente entre el calor específico a presión constante y el calor específico a volumen constante se denomina coeficiente de dilatación adiabática (a menudo denotado γ gamma).[9] Este parámetro aparece en fórmulas físicas como por ejemplo la de la velocidad del sonido en un gas ideal. El calor específico de las sustancias moleculares (distintas de los gases monoatómicos) no está dado por constantes fijas y puede variar un poco dependiendo de la temperatura [2]. Por lo tanto, la temperatura a la cual se hace la medición debe especificarse con precisión. Algunos ejemplos son los siguientes: Agua (líquido): cp = 4.1855 J g–1 K–1 (15 °C) La presión a la cual el calor específico se mide es especialmente importante para gases y líquidos. El estándar de presión fue hasta 1982 1 atmósfera, que está definida como el equivalente de la presión atmosférica al nivel del mar o sea exactamente 101.325 kPa o 760 Torr. A partir de ese año, la IUPAC recomendó que para propósitos de especificar las propiedades físicas de las sustancias "el estándar de presión" debía definirse como exactamente 100 kPa o (≈750.062 Torr). Aparte de ser un número redondo, este cambio tiene una ventaja práctica porque 100 kPa equivalen a una altitud aproximada de 112 metros, que está cercana al promedio de 194 m de de la población mundial.[10] Factores que afectan el calor específico
Grados de libertadLas moléculas son bastante diferentes de los gases monoatómicos como el helio o el hidrógeno. Con los gases monoatómicos, la energía calorífica se almacena únicamente en movimientos traslacionales. Los movimientos traslacionales son, por lo general, movimientos de cuerpo completo en un espacio tridimensional en el que las partículas se mueven e intercambian energía en colisiones en forma similar a como lo harían pelotas de goma encerradas en un recipiente que se agitaran con fuerza. (vea la animación aquí). Estos movimientos simples en los ejes dimensionales X, Y, y Z implican que los gases monoatómicos sólo tienen tres grados de libertad traslacionales. Las moléculas, en cambio, tienen varios grados de libertad internos y rotacionales adicionales ya que son objetos complejos; son una población de átomos que se pueden mover dentro de una molécula de distintas formas (ver la animación a la derecha). La energía calorífica se almacena en estos movimientos internos. Por ejemplo, el Nitrógeno, que es una molécula diatómica, tiene cinco grados de libertad disponibles: los tres traslacionales más dos rotacionales de libertad interna. Notablemente la capacidad calorífica a volumen constante de los gases monoatómicos es Masa molarUna de las razones por las que el calor específico adopta diferentes valores para diferentes sustancias es la diferencia en masas molares, que es la masa de un mol de cualquier elemento, la cual es directamente proporcional a la masa molecular del elemento, suma de los valores de las masas atómicas de la molecula en cuestion. La energía calorífica se almacena gracias a la existencia de átomos o moléculas vibrando. Si una sustancia tiene una masa molar más ligera, entonces cada gramo de ella tiene más átomos o moléculas disponible para almacenar energía. Es por esto que el hidrógeno, la sustancia con la menor masa molar, tiene un calor específico tan elevado; porque un gramo de esta sustancia contiene una cantidad tan grande de moléculas. Una consecuencia de este fenómeno es que, cuando se mide el calor específico en términos molares la diferencia entre sustancias se hace menos pronunciada, y el calor específico del hidrógeno deja de ser atípico. En forma correspondiente, las sustancias moleculares (que también absorben calor en sus grados internos de libertad), pueden almacenar grandes cantidades de energía por mol si se trata de moléculas grandes y complejas, y en consecuencia su calor específico medido en términos másicos es menos notable. Ya que la densidad neta de un elemento químico está fuertemente relacionada con su masa molar, existe en términos generales, una fuerte correlación inversa entre la densidad del sólido y su cp (calor específico a presión constante medido en términos másicos). Grandes lingotes de sólidos de baja densidad tienden a absorber más calor que un lingote pequeño de un sólido de la misma masa pero de mayor densidad ya que el primero por lo general contiene más átomos. En consecuencia, en términos generales, hay una correlación cercana entre el volumen de un elemento sólido y su capacidad calorífica total. Hay sin embargo, muchas desviaciones de esta correlación general. Enlaces puente de hidrógenoLas moléculas que contienen enlaces polares de hidrógeno tienen la capacidad de almacenar energía calorífica en éstos enlaces, conocidos como puentes de hidrógeno. ImpurezasEn el caso de las aleaciones, hay ciertas condiciones en las cuales pequeñas impurezas pueden alterar en gran medida el calor específico medido. Las aleaciones pueden mostrar una marcada diferencia en su comportamiento incluso si la impureza en cuestión es uno de los elementos que forman la aleación; por ejemplo, las impurezas en aleaciones semiconductoras ferromagnéticas pueden llevar a mediciones muy diferentes, tal como predijeron por primera vez White y Hogan.[11] Tabla de calores específicos
↑ Divida el calor específico másico del Magnesio entre 8 y comprobará que es muy cercano a ocho veces el del Plomo. ↑ Asumiendo una altitud de 194 metros (el promedio de la población mundial), una temperatura de 23 °C, un 40,85% de humedad y 760 mmHg de presión. ↑ Puede notar que el calor específico (molar) de los gases monoatómicos se comporta de acuerdo a ciertas constantes, mientras que los valores predichos para otros gases no se ajustan con la misma precisión. Materiales de construcciónÉstos datos son de utilidad al calcular los efectos del calor sobre los materiales:
Véase también
Referencias
Enlaces externos
Categoría: Calorimetría |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Este articulo se basa en el articulo Calor_específico publicado en la enciclopedia libre de Wikipedia. El contenido está disponible bajo los términos de la Licencia de GNU Free Documentation License. Véase también en Wikipedia para obtener una lista de autores. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||





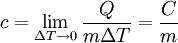
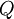 es el calor que se entra o sale de la sustancia,
es el calor que se entra o sale de la sustancia, 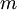 es la masa (se usa una n cuando la medición es
es la masa (se usa una n cuando la medición es 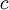 es el calor específico de la sustancia, y
es el calor específico de la sustancia, y 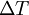 es el incremento de temperatura.
es el incremento de temperatura.
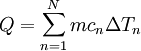
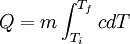
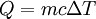
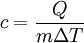
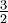
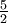 R, lo cual muestra claramente la relación entre los grados de libertad y el calor específico.
R, lo cual muestra claramente la relación entre los grados de libertad y el calor específico.