El enigma del platino
Cómo se produce una reacción química que, a primera vista, no debería ser posible a las temperaturas observadas
Anuncios
¿Qué ocurre cuando un gato se sube a un girasol? El girasol es inestable, se doblará rápidamente y el gato caerá al suelo. Sin embargo, si el gato sólo necesita un rápido impulso para coger un pájaro desde allí, entonces el girasol puede actuar como un "paso intermedio metaestable". Este es, en esencia, el mecanismo por el que los átomos individuales de un catalizador capturan moléculas para transformarlas químicamente.
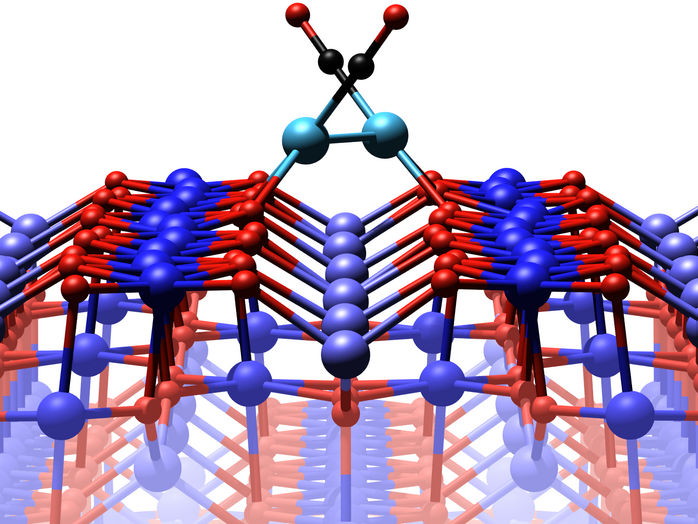
La superficie de óxido de hierro con dos átomos de platino, cada uno de los cuales está unido a una molécula de monóxido de carbono.
Technische Universität Wien
Hace varios años, el grupo de física de superficies de la TU Wien descubrió que los catalizadores de platino de "átomos individuales" podían oxidar el monóxido de carbono a temperaturas que, según sus modelos teóricos, no deberían haber sido posibles. Ahora, con la ayuda de imágenes de microscopio a escala atómica y complejas simulaciones por ordenador, han podido demostrar que tanto el propio catalizador como el material en el que está anclado asumen estados "metaestables" energéticamente desfavorables durante un breve periodo de tiempo para permitir que la reacción se produzca de forma especial. Los resultados se han publicado en la revista Science Advances.
Átomos individuales como catalizadores
El grupo de investigación del profesor Gareth Parkinson, del Instituto de Física Aplicada de la Universidad Técnica de Viena, está investigando los catalizadores más pequeños posibles: Se colocan átomos individuales de platino en una superficie de óxido de hierro. A continuación, entran en contacto con el gas monóxido de carbono y se convierten en dióxido de carbono, como ocurre en el tubo de escape de un coche moderno.
"Este proceso es técnicamente muy importante, pero hasta ahora no estaba claro qué ocurre exactamente cuando el catalizador se reduce de tamaño hasta el límite de un solo átomo", dice Gareth Parkinson. "En nuestro grupo de investigación, estudiamos estos procesos de varias maneras: por un lado, utilizamos un microscopio de barrido en túnel para producir imágenes de altísima resolución en las que se puede estudiar el movimiento de los átomos individuales. Y por otro lado, analizamos el proceso de reacción con espectroscopia y simulaciones por ordenador".
Que los átomos de platino sean activos como catalizadores depende de la temperatura. En el experimento, el catalizador se calienta lenta y uniformemente hasta que se alcanza la temperatura crítica y el monóxido de carbono se convierte en dióxido de carbono. Ese umbral es de unos 550 Kelvin. "Sin embargo, esto no se ajustaba a nuestras simulaciones informáticas originales", dice Matthias Meier, primer autor de la actual publicación. "Según la teoría del funcionamiento de la densidad, que se utiliza normalmente para este tipo de cálculos, el proceso sólo podía tener lugar a 800 Kelvin. Así que lo supimos: hasta ahora se había pasado por alto algo importante".
Un estado metaestable: de corta duración, pero importante
Durante varios años, el equipo acumuló una amplia experiencia con los mismos materiales en otras reacciones y, como resultado, surgió una nueva imagen paso a paso. "Con la teoría del funcional de la densidad, normalmente se calcula el estado del sistema que tiene la energía más baja", dice Matthias Meier. "Eso tiene sentido, porque ese es el estado que el sistema asume con más frecuencia. Pero en nuestro caso, hay un segundo estado que desempeña un papel fundamental: El llamado estado metaestable".
Tanto los átomos de platino como la superficie de óxido de hierro pueden alternar entre diferentes estados físicos cuánticos. El estado básico, con la energía más baja, es estable. Cuando el sistema pasa al estado metaestable, vuelve inevitablemente al estado básico al cabo de poco tiempo, como el gato que intenta llegar a la cima en un palo de escalada inestable. Pero en la conversión catalítica del monóxido de carbono, basta con que el sistema esté en el estado metaestable durante un tiempo muy breve: Al igual que un breve momento en un estado de escalada inestable puede ser suficiente para que el gato atrape un pájaro con su pata, el catalizador puede convertir el monóxido de carbono en el estado metaestable.
Cuando se introduce el monóxido de carbono por primera vez, dos átomos de platino se unen para formar un dímero. Cuando la temperatura es lo suficientemente alta, el dímero puede pasar a una posición menos favorable en la que los átomos de oxígeno de la superficie están menos débilmente unidos. En el estado metaestable, el óxido de hierro cambia su estructura atómica precisamente en este punto, liberando el átomo de oxígeno que el óxido de carbono necesita para formar dióxido de carbono, que sale volando al instante, completando el proceso de catálisis. "Si incluimos en nuestra simulación por ordenador estos estados a corto plazo que antes no se tenían en cuenta, obtenemos exactamente el resultado que también se midió en el experimento", afirma Matthias Meier.
"El resultado de nuestra investigación demuestra que en la física de superficies a menudo se necesita mucha experiencia", dice Gareth Parkinson. "Si no hubiéramos estudiado procesos químicos muy diferentes a lo largo de los años, probablemente nunca habríamos resuelto este enigma". Recientemente, la inteligencia artificial también se ha utilizado con gran éxito para analizar los procesos químicos cuánticos, pero en este caso, está convencido Parkinson, probablemente no habría tenido éxito. Para llegar a soluciones creativas fuera de lo que se creía posible, probablemente se necesiten seres humanos, después de todo.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.