PFAS: una vía novedosa para acabar con las "sustancias químicas para siempre"
Se ha desarrollado un nuevo catalizador capaz de escindir fuertes enlaces carbono-flúor: posible uso en la producción farmacéutica
Anuncios
Químicos de la Universidad Goethe de Fráncfort han desarrollado un catalizador capaz de descomponer de forma selectiva sustancias orgánicas perfluoradas y polifluoradas (PFAS), también conocidas como "sustancias químicas para siempre". Los PFAS se utilizan mucho para hacer superficies resistentes a la suciedad y el agua, pero su extrema persistencia en el medio ambiente y sus posibles riesgos para la salud los han convertido en una preocupación creciente. Lo que diferencia a este nuevo catalizador es que no depende de metales pesados costosos o tóxicos como el platino, el paladio o el iridio. Además de su capacidad para degradar los PFAS, el catalizador también podría utilizarse en la síntesis de productos farmacéuticos.
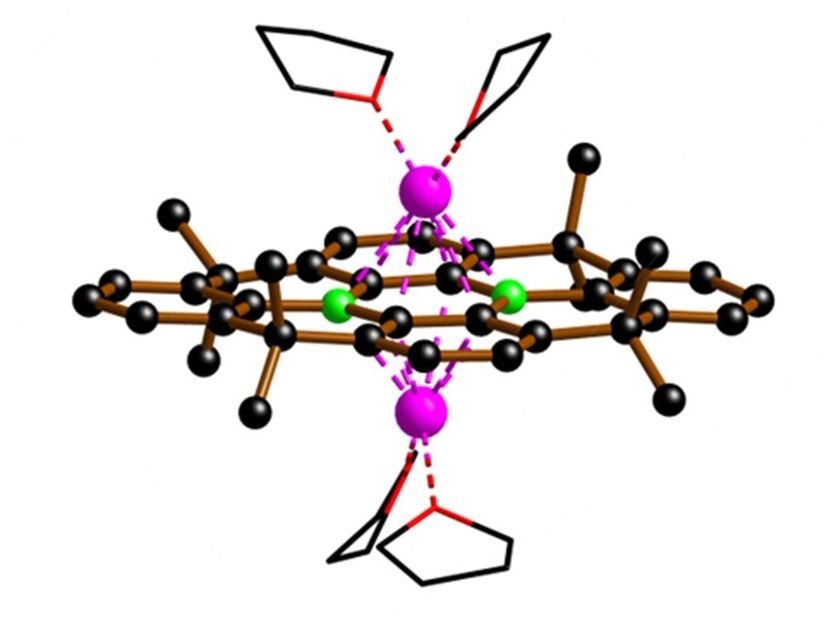
Un nuevo catalizador rompe los enlaces C-F: Dos átomos de boro (esferas verdes) están incrustados en una estructura de átomos de carbono (negro). Los electrones necesarios para escindir los enlaces C-F proceden actualmente del litio (rosa) y en el futuro de la corriente eléctrica.
Gruppe von Matthias Wagner, Goethe-Universität Frankfurt
Los PFAS son, en muchos sentidos, moléculas extraordinarias. Incluso una fina capa puede repeler el agua, el aceite y la suciedad. También son muy resistentes al calor y a la luz ultravioleta, por lo que son ideales para recubrir ropa transpirable de exterior, alfombras resistentes a las manchas, vajillas desechables, planchas y sartenes antiadherentes. Industrialmente, los PFAS se utilizan como lubricantes, tensioactivos, agentes humectantes, en el cromado y en espumas contra incendios. La lista continúa: los PFAS están prácticamente en todas partes.
Pero estas ventajas tienen un coste: como los PFAS son tan resistentes, persisten en el medio ambiente mucho después de su uso previsto. Aunque pueden destruirse casi por completo en las plantas de incineración de residuos, pueden acumularse en el ciclo de los materiales durante el reciclado -incluidos los textiles o los lodos de depuradora- y pasar al medio ambiente. Los PFAS pueden encontrarse en el agua, el suelo, las plantas e incluso en el cuerpo humano. Esto es especialmente preocupante porque se sospecha que algunos de los aproximadamente 4.700 compuestos de PFAS conocidos son cancerígenos o causan otros problemas de salud.
La clave de la eficacia de los PFAS -y de su persistencia en el medio ambiente- reside en su estructura molecular extremadamente estable, especialmente en los enlaces carbono-flúor (C-F). Ahora, un equipo de químicos dirigido por el profesor Matthias Wagner, del Instituto de Química Inorgánica y Analítica de la Universidad Goethe, ha desarrollado un catalizador capaz de romper estos enlaces C-F en cuestión de segundos y a temperatura ambiente. El núcleo del catalizador está formado por dos átomos de boro incrustados en una estructura de carbono que los hace resistentes al aire y la humedad, una propiedad poco común y muy práctica en los compuestos de boro.
Christoph Buch, investigador doctoral del grupo de Wagner y primer autor del estudio, explica: "Para romper enlaces C-F necesitamos electrones, que nuestro catalizador transfiere con una eficacia excepcional. Hasta ahora, hemos utilizado metales alcalinos como el litio como fuente de electrones, pero ya estamos trabajando para cambiarlos por corriente eléctrica. Eso simplificaría mucho el proceso y lo haría más eficiente".
Más allá de la degradación de PFAS, Wagner ve aplicaciones más amplias para el catalizador: "Muchas sustancias farmacológicamente importantes contienen átomos de flúor para aumentar su estabilidad fisiológica y potenciar su efecto. Los átomos de flúor también pueden mejorar la absorción de los fármacos. Con este catalizador, disponemos ahora de una herramienta que nos permite controlar con precisión el grado de fluoración de tales compuestos."
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.
Publicación original
Christoph D. Buch, Alexander Virovets, Eugenia Peresypkina, Burkhard Endeward, Hans-Wolfram Lerner, Felipe Fantuzzi, Shigehiro Yamaguchi, Matthias Wagner; "Planarity Is Not Plain: Closed- vs Open-Shell Reactivity of a Structurally Constrained, Doubly Reduced Arylborane toward Fluorobenzenes"; Journal of the American Chemical Society, Volume 147, 2025-5-29