Un método sencillo destruye las peligrosas "sustancias químicas para siempre", haciendo que el agua sea segura
Utilizando reactivos comunes en agua calentada, los químicos pueden "descabezar" y descomponer los PFAS, dejando sólo los compuestos inocuos
Anuncios
Si le desesperan los recientes informes de que las fuentes de agua de la Tierra se han infestado a fondo con sustancias químicas peligrosas fabricadas por el hombre, llamadas PFAS, que pueden durar miles de años, haciendo que incluso el agua de lluvia sea insegura para beber, hay una buena noticia.

Imagen simbólica
pixabay.com
Químicos de la UCLA y la Universidad de Northwestern han desarrollado una forma sencilla de descomponer casi una docena de estos "productos químicos para siempre" casi indestructibles a temperaturas relativamente bajas y sin subproductos nocivos.
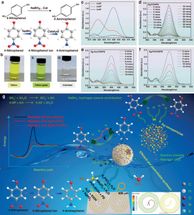
En un artículo publicado en la revista Science, los investigadores demuestran que en agua calentada a sólo 176 a 248 grados Fahrenheit, los disolventes y reactivos comunes y baratos rompieron los enlaces moleculares de los PFAS que se encuentran entre los más fuertes conocidos e iniciaron una reacción química que "mordisqueó gradualmente la molécula" hasta que desapareció, dijo el distinguido profesor de investigación de la UCLA y coautor de la investigación, Kendall Houk.
La sencillez de la tecnología, las temperaturas comparativamente bajas y la ausencia de subproductos nocivos significan que no hay límite a la cantidad de agua que puede procesarse a la vez, añadió Houk. La tecnología podría facilitar a las plantas de tratamiento de agua la eliminación de los PFAS del agua potable.
Las sustancias perfluoroalquiladas y polifluoroalquiladas (PFAS) son una clase de unas 12.000 sustancias químicas sintéticas que se utilizan desde la década de 1940 en utensilios de cocina antiadherentes, maquillaje resistente al agua, champús, productos electrónicos, envases de alimentos y otros muchos productos. Contienen un enlace entre átomos de carbono y flúor que nada en la naturaleza puede romper.
Cuando estas sustancias químicas se filtran al medio ambiente a través de la fabricación o el uso cotidiano de los productos, pasan a formar parte del ciclo del agua de la Tierra. En los últimos 70 años, los PFAS han contaminado prácticamente todas las gotas de agua del planeta, y su fuerte vínculo entre el carbono y el flúor les permite pasar por la mayoría de los sistemas de tratamiento del agua sin sufrir ningún daño. Pueden acumularse en los tejidos de las personas y los animales a lo largo del tiempo y causar daños en formas que los científicos apenas están empezando a comprender. Algunos cánceres y enfermedades de la tiroides, por ejemplo, están asociados a los PFAS.
Por estas razones, es especialmente urgente encontrar formas de eliminar los PFAS del agua. Los científicos están experimentando con muchas tecnologías de remediación, pero la mayoría de ellas requieren temperaturas extremadamente altas, productos químicos especiales o luz ultravioleta y a veces producen subproductos que también son perjudiciales y requieren pasos adicionales para su eliminación.
Llevar los PFAS a la guillotina
El profesor de química de Northwestern William Dichtel y la estudiante de doctorado Brittany Trang se dieron cuenta de que, mientras las moléculas de PFAS contienen una larga "cola" de persistentes enlaces carbono-flúor, su grupo "cabeza" suele contener átomos de oxígeno cargados, que reaccionan fuertemente con otras moléculas. El equipo de Dichtel construyó una guillotina química calentando los PFAS en agua con dimetilsulfóxido, también conocido como DMSO, e hidróxido de sodio, o lejía, que cortó la cabeza y dejó al descubierto una cola reactiva.
"Eso desencadenó todas estas reacciones y empezó a escupir átomos de flúor de estos compuestos para formar fluoruro, que es la forma más segura de flúor", dijo Dichtel. "Aunque los enlaces carbono-flúor son superfuertes, ese grupo de cabeza cargado es el talón de Aquiles".
Pero los experimentos revelaron otra sorpresa: Las moléculas no parecían deshacerse como la sabiduría convencional decía que debían hacerlo.
Para resolver este misterio, Dichtel y Trang compartieron sus datos con sus colaboradores Houk y Yuli Li, estudiante de la Universidad de Tianjin, que trabajaba en el grupo de Houk a distancia desde China durante la pandemia. Los investigadores esperaban que las moléculas de PFAS se desintegraran de un átomo de carbono cada vez, pero Li y Houk realizaron simulaciones por ordenador que mostraron que dos o tres moléculas de carbono se desprendían de las moléculas simultáneamente, tal y como Dichtel y Tang habían observado experimentalmente.
Las simulaciones también mostraron que los únicos subproductos debían ser el flúor -que suele añadirse al agua potable para prevenir las caries-, el dióxido de carbono y el ácido fórmico, que no es perjudicial. Dichtel y Trang confirmaron estos subproductos previstos en otros experimentos.
"Se trató de un conjunto de cálculos muy complejos que pusieron a prueba los métodos de mecánica cuántica más modernos y los ordenadores más rápidos de los que disponemos", dijo Houk. "La mecánica cuántica es el método matemático que simula toda la química, pero sólo en la última década hemos sido capaces de enfrentarnos a grandes problemas mecanicistas como éste, evaluando todas las posibilidades y determinando cuál puede ocurrir a la velocidad observada".
Según Houk, Li domina estos métodos computacionales y ha trabajado a larga distancia con Trang para resolver este problema fundamental pero de gran importancia práctica.
El trabajo actual degrada 10 tipos de ácidos perfluoroalquilos carboxílicos (PFCA) y ácidos perfluoroalquilos carboxílicos (PFECA), incluido el ácido perfluorooctanoico (PFOA). Los investigadores creen que su método funcionará para la mayoría de los PFAS que contienen ácidos carboxílicos y esperan que ayude a identificar puntos débiles en otras clases de PFAS. Esperan que estos resultados alentadores conduzcan a nuevas investigaciones que pongan a prueba métodos para erradicar los miles de otros tipos de PFAS.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.
Publicación original
Brittany Trang et al.; Low-temperature mineralization of perfluorocarboxylic acids; Science; 2022