Fotografiadas 'in fraganti' las sustancias intermedias de una reacción química
Investigadores de la UPV/EHU captan por primera vez la imagen de todas las etapas de una compleja reacción orgánica y resuelven los mecanismos que la explican
Anuncios
Uno de los objetivos que durante muchísimo tiempo han perseguido los químicos ha sido ser capaces de poder seguir y visualizar directamente cómo cambian las estructuras de las moléculas cuando experimentan complejas transformaciones químicas. Los intermedios de reacción - sustancias muy inestables que se forman en las diferentes etapas de una reacción, antes de obtener los productos - son extremadamente difíciles de identificar y caracterizar, debido a su corta vida. Conocer la estructura de estas especies intermedias puede ser de gran ayuda para entender los mecanismos de la reacción, y eso, además, puede generar un gran impacto en la industria química, la ciencia de materiales, la nanotecnología, la biología y la medicina.
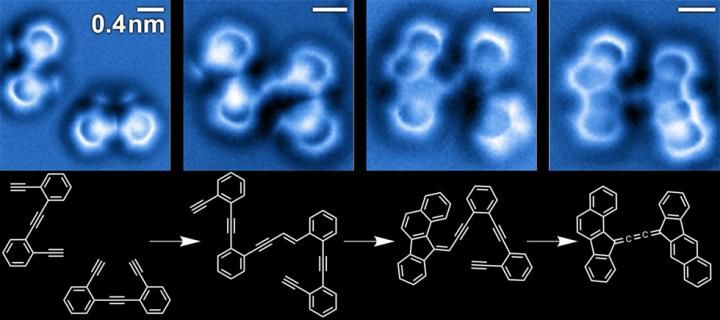
Secuencia de imágenes de las etapas de la reacción de moléculas de enediina sobre una superficie de plata.
A. Riss / Technische Universität München
Un equipo internacional de investigadores liderados por Felix R. Fischer y Michael F. Crommie (Universidad de California en Berkeley y Lawrence Berkeley National Laboratory) y por Ángel Rubio (catedrático de la UPV/EHU, líder del grupo de investigación Nano-Bio Spectroscopy Group de la UPV/EHU y director del Max Planck Institute for the Structure and Dynamics of Matter de Hamburgo) ha captado la imagen y ha resuelto la configuración de los enlaces de los reactivos, de los intermedios y de los productos finales de una compleja reacción orgánica, a nivel de una sola molécula. Nature Chemistry ha publicado la investigación en su último número.
El equipo ha conseguido las imágenes de las estructuras químicas asociadas a diferentes etapas de la reacción en cascada, de múltiples etapas, de moléculas de enediina sobre una superficie de plata, utilizando un microscopio de fuerza atómica sin contacto (nc-AFM, por sus siglas en inglés) con una sonda especialmente sensible: utiliza una aguja muy fina que puede detectar las más pequeñas protuberancias a escala atómica (de una manera similar a la lectura en Braille), ya que se adsorbe una molécula de monóxido de carbono que actúa como "dedo" en la lectura, para aumentar su resolución.
La identificación precisa de la configuración de enlaces de las especies intermedias "ha permitido determinar la compleja secuencia de transformaciones químicas a lo largo del mecanismo de reacción, partiendo de los reactivos, pasando por los intermedios y acabando en los productos finales - explica Ángel Rubio, catedrático de la UPV/EHU -, y, a su vez, ha permitido resolver los mecanismos microscópicos que suceden en este comportamiento dinámico tan complejo".
Estabilización de intermedios
Mediante la combinación de los últimos avances en cálculo numérico y los modelos analíticos clásicos que describen la cinética de reacciones químicas secuenciales - área que estudia la rapidez de las reacciones y los eventos moleculares que suceden en ella -, ha quedado probado que, para explicar la estabilización de las sustancias intermedias, no es suficiente considerar la energía potencial de las mismas, sino que es fundamental tener en cuenta la disipación de energía y los cambios de entropía molecular - la entropía mide el grado de organización de un sistema -. La superficie, y en particular la interacción de las sustancias intermedias extremadamente inestables con la superficie, juega un papel fundamental tanto en la entropía como en la disipación de energía, que marca una gran diferencia entre las reacciones soportadas en una superficie y las reacciones en fase gaseosa o en disolución.
Esta detallada comprensión, conseguida gracias a la sinergia entre la visualización de las reacciones químicas de una molécula y los últimos avances en modelización computacional, "constituye un hito fundamental en el análisis de las reacciones químicas", concreta. De hecho, con todo ello, "se han superado muchas de las limitaciones de las técnicas espectroscópicas convencionales - afirma -, y se ha conseguido una imagen a escala atómica, sin precedentes, de los mecanismos de reacción, las fuerzas impulsoras y la cinética". Según explica Rubio, todo este nuevo conocimiento puede abrir incontables nuevos campos, nunca explorados hasta el momento: futuros diseños y optimizaciones de sistemas catalíticos heterogéneos, desarrollo de nuevas herramientas de síntesis aplicadas a la nanotecnología del carbono, así como aplicaciones en ciencias de materiales y bioquímicas.















































