|
|
| Nombre (IUPAC) sistemático
|
| tetraoxosulfato (VI) de zinc
|
| General
|
| Otros nombres | Vitriolo blanco, Goslarita, vitriolo de Goslar
|
| Fórmula semidesarrollada
| ZnSO4 (anhidro)
ZnSO4.H2O (monohidrato)
ZnSO4.6 H2O (hexahidrato)
ZnSO4.7 H2O (heptahidrato)
|
| Fórmula molecular | ZnSO4
|
| Identificadores
|
| Número CAS
| 7733-02-0 (sal anhidra)
7446-19-7 (monohidrato)
13986-24-8 (hexahidrato)
7446-20-0 (heptahidrato)
|
| Propiedades físicas
|
| Estado de agregación | Sólido
|
| Apariencia | Polvo blanco cristalino, inodoro.
|
| Densidad
| 3,74×10³ (anhidro)
kg/m3; 1,957 (Heptahidrato)[1] g/cm3
|
| Masa
| 161,454 (anhidro)
287,55 (heptahidrato) u
|
| Punto de fusión
| 373 K (100 °C)
|
| Punto de ebullición
| Se descompone por encima de 773 K (500 °C)
|
| Propiedades químicas
|
| Solubilidad en agua
| Muy soluble en agua. Soluble en metanol y glicerol. Ligeramente soluble en etanol
|
| KPS
| n/d
|
| Termoquímica
|
| ΔfH0sólido | -982,8 kJ/mol
|
| S0sólido | 110.5 J·mol-1·K-1
|
| Peligrosidad
|
| Frases R | R22- Nocivo por ingestión.
R41- Riesgo de lesiones oculares graves.
R50- Muy tóxico para los organismos acuáticos.
R53 Puede provocar a largo plazo efectos negativos en el medio ambiente acuático.
|
| Frases S | S2- Manténgase fuera del alcance de los niños.
S22- No respirar el polvo.
S26- En caso de contacto con los ojos, lávense inmediata y abundantemente con agua y acúdase a un médico.
S39- Úsese protección para los ojos/la cara.
S46- En caso de ingestión, acúdase inmediatamente al médico y muéstrele la etiqueta o el envase.
S60- Elimínense el producto y su recipiente como residuos peligrosos.
S61- Evítese su liberación al medio ambiente. Recábense instrucciones específicas de la ficha de datos de seguridad.
|
| Riesgos
|
| Ingestión | Nocivo leve. Dolor abdominal, náuseas, vómitos y diarrea.
Irritaciones en la boca y tracto digestivo. Daño a los riñones. Pancreatitis.
En casos extremos, convulsiones, variaciones de presión y coma.
Dosis letal humano: 180 mg/kg (Zinc Sulfato Anhidro).
|
| Inhalación | Irritaciones en el tracto respiratorio. Tos y dificultad respiratoria.
|
| Piel | Irritaciones. Enrojecimiento, picazón y dolor.
|
| Ojos | Irritaciones. Enrojecimiento y dolor.
|
| LD50 | DL50 (oral - rata): 2949 mg/kg (Zinc Sulfato Anhidro).
|
| Más información | Hazardous Chemical Database
|
Valores en el SI y en condiciones normales
(0 °C y 1 atm), salvo que se indique lo contrario.
Exenciones y referencias
|
El sulfato de zinc es un compuesto químico cristalino, incoloro y soluble en agua, de fórmula ZnSO4, aunque siempre va acompañado de un determinado número de moléculas de agua de hidratación.
Formas hidratadas y anhidra
Suele presentarse como sal heptahidratada, ZnSO4·7H2O.
A 30 ºC pierde una molécula de agua y se transforma en ZnSO4·6H2O.[2]
A 70 ºC pierde otras cinco moléculas de agua y se transforma en ZnSO4·H2O. Finalmente, a 280 ºC pierde la última molécula de agua y se transforma en la sal anhidra.[3]
Obtención
En la Naturaleza se presenta formando parte del mineral goslarita (heptahidrato), conocido también como "vitriolo blanco" y de la bianchita (hexahidrato). Puede prepararse por reacción de zinc o del óxido de zinc con ácido sulfúrico en disolución acuosa.
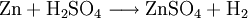
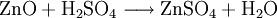
O por oxidación enérgica del sulfuro de zinc, componente de la blenda.
 . .
También puede prepararse añadiendo zinc sólido a disoluciones de sulfato de cobre (II) o sulfato de hierro (II).
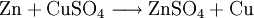 . .
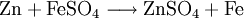 . .
Usos
Se usa como suplemento de zinc en la alimentación animal, para preparar abonos y sprays agrícolas. ZnSO4·7H2O se usa en fabricación de litopón (blanco de zinc), y rayón (seda artificial), como conservante de madera, como ][electrolito]]s para plateado con cinc (cincado), como mordiente de coloración, para preservar pieles y cuero, y en Medicina, como astringente y emético.
Una disolución acuosa de sulfato de zinc resulta efectiva para eliminar musgo de los pavimentos y suelos.
[4]
Se han referido usos del sulfato de zinc para enmascarar las pruebas y análisis antidroga porque actúa como quelante de las moléculas, retirándolas de la orina.[5]
Enlaces externos
- Instituto Nacional de Seguridad e Higiene en el Trabajo de España: Ficha internacional de seguridad química del sulfato de zinc.
- [4] http://www.chemblink.com/products/7733-02-0.htm
- [5] Extracto delmanual Merck, consultado en http://www.hbci.com/~wenonah/hydro/znso.htm
Referencias
- ↑ BGIA GESTIS: Base de datos de sustancias peligrosas; ZVG=1440. Consultado en [1] el 11 de Abril de 2008
- ↑ Zinc Sulfate
- ↑ Kaye and Laby. Table of physical and chemical constants. National Physical Laboratory
- ↑ http://bryophytes.science.oregonstate.edu/page24.htm [2]
- ↑ http://www.totse.com/en/drugs/legal_issues_of_drug_use/urinetst.html [3]
|





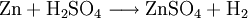
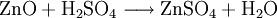
 .
.
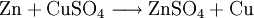 .
.
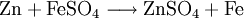 .
.


