La reacción química más fría
Con la química ultra-fría, los investigadores obtienen una primera visión de lo que sucede exactamente durante una reacción química
Anuncios
La reacción química más fría en el universo conocido tuvo lugar en lo que parece ser un caótico lío de láseres. La apariencia engaña: En lo profundo de ese caos cuidadosamente organizado, a temperaturas millones de veces más frías que en el espacio interestelar, Kang-Kuen Ni logró una hazaña de precisión. Forzando a dos moléculas ultracongeladas a encontrarse y reaccionar, rompió y formó los enlaces más fríos en la historia de los acoplamientos moleculares.
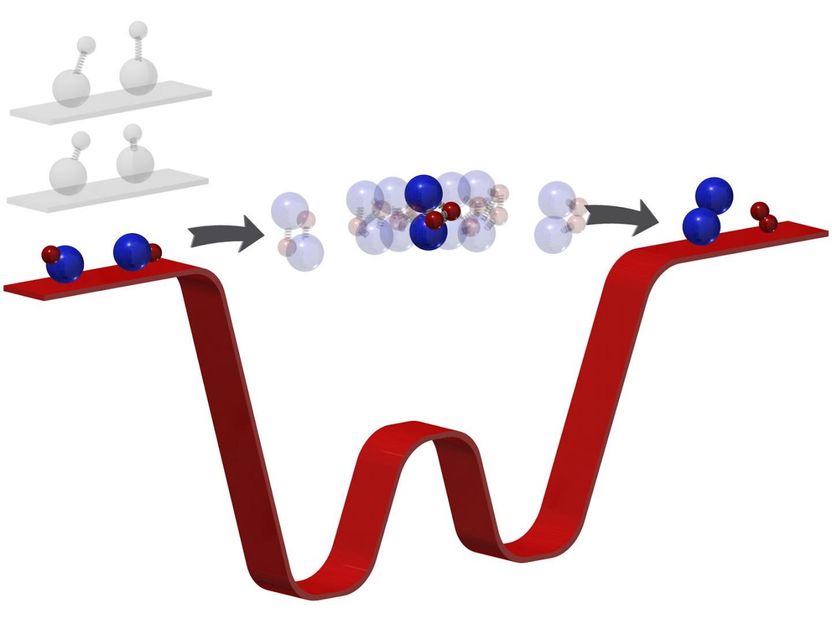
Las reacciones químicas transforman los reactivos en productos a través de un estado intermedio donde los enlaces se rompen y se forman. A menudo demasiado efímera para ser observada, esta fase ha eludido hasta tal punto la investigación íntima. Al "congelar" la rotación, vibración y movimiento de los reactivos (aquí, moléculas de potasio-rubidio) a una temperatura de 500 nanocelvin (apenas por encima de la temperatura cero absoluta), el número de salidas energéticamente permitidas para los productos es limitado. "Atrapados" en el intermedio durante mucho más tiempo, los investigadores pueden entonces observar esta fase directamente con la detección de fotoionización. Esta técnica allana el camino hacia el control cuántico de las reacciones químicas con moléculas ultrafrías.
Ming-Guang Hu
"Probablemente en los próximos dos años, somos el único laboratorio que puede hacer esto", dijo Ming-Guang Hu, un erudito postdoctoral en el laboratorio de Ni y primer autor en su artículo publicado en Science. Hace cinco años, Ni, el Profesor Asociado de Química y Biología Química de Morris Kahn y pionero de la química ultra fría, se propuso construir un nuevo aparato que pudiera lograr las reacciones químicas a la temperatura más baja de cualquier tecnología disponible actualmente. Pero no podían estar seguros de que su intrincada ingeniería funcionaría.
Ahora, no sólo realizaron la reacción más fría hasta ahora, sino que descubrieron que su nuevo aparato puede hacer algo que ni siquiera predijeron. En un frío tan intenso, 500 nanocelvin o unas pocas millonésimas de grado por encima de cero absoluto, sus moléculas se ralentizaron a velocidades glaciales, Ni y su equipo pudieron ver algo que nadie había podido ver antes: el momento en que dos moléculas se encuentran para formar dos nuevas moléculas. En esencia, capturaron una reacción química en su acto más crítico y elusivo.
Las reacciones químicas son responsables de literalmente todo: respirar, cocinar, digerir, crear energía, productos farmacéuticos y productos para el hogar como el jabón. Por lo tanto, comprender cómo funcionan a un nivel fundamental podría ayudar a los investigadores a diseñar combinaciones que el mundo nunca ha visto. Con un número casi infinito de nuevas combinaciones posibles, estas nuevas moléculas podrían tener infinitas aplicaciones, desde la producción de energía más eficiente hasta nuevos materiales como paredes a prueba de moho e incluso mejores bloques de construcción para computadoras cuánticas.
En su trabajo anterior, Ni utilizó temperaturas más frías y más frías para hacer funcionar esta magia química: forjar moléculas a partir de átomos que de otro modo nunca reaccionarían. Enfriados hasta tales extremos, los átomos y las moléculas se vuelven lentos hasta llegar a un arrastre cuántico, su estado de energía más bajo posible. Allí, el Ni puede manipular las interacciones moleculares con la máxima precisión. Pero incluso ella sólo podía ver el comienzo de sus reacciones: dos moléculas entran, ¿pero luego qué? Lo que sucedió en el medio y al final fue un agujero negro que sólo las teorías podían tratar de explicar.
Las reacciones químicas ocurren en tan sólo una millonésima de milmillonésima de segundo, más conocidas en el mundo científico como femtosegundos. Incluso la tecnología más sofisticada de hoy en día no puede capturar algo tan efímero, aunque algunos se acercan. En los últimos veinte años, los científicos han utilizado láseres ultrarrápidos como cámaras de acción rápida, que captan imágenes rápidas de las reacciones a medida que ocurren. Pero no pueden capturar toda la imagen. La mayor parte del tiempo", dijo Ni, "sólo se ve que los reactivos desaparecen y los productos aparecen en un tiempo que se puede medir". No había una medición directa de lo que realmente sucedió en estas reacciones químicas". Hasta ahora.
Las temperaturas ultra-frías de Ni fuerzan las reacciones a una velocidad comparativamente adormecida. "Porque[las moléculas] son tan frías", dijo Ni, "ahora tenemos un efecto de cuello de botella". Cuando ella y su equipo reaccionaron dos moléculas de rubidio de potasio, elegidas por su flexibilidad, las temperaturas ultra-frías forzaron a las moléculas a permanecer en la etapa intermedia durante microsegundos. Los microsegundos -mero millonésima parte de un segundo- pueden parecer cortos, pero eso es millones de veces más largo de lo normal y lo suficiente para que Ni y su equipo investiguen la fase en la que los enlaces se rompen y forman, en esencia, cómo una molécula se convierte en otra.
Con esta visión íntima, Ni dijo que ella y su equipo pueden probar teorías que predicen lo que sucede en el agujero negro de una reacción para confirmar si lo hicieron bien. Entonces, su equipo puede elaborar nuevas teorías, utilizando datos reales para predecir con mayor precisión lo que sucede durante otras reacciones químicas, incluso aquellas que tienen lugar en el misterioso reino cuántico.
El equipo ya está explorando qué más pueden aprender en su banco de pruebas ultracrío. Luego, por ejemplo, podrían manipular los reactivos, excitándolos antes de que reaccionen para ver cómo su energía aumentada impacta el resultado. O bien, podrían incluso influir en la reacción a medida que ésta se produce, empujando una molécula u otra. "Con nuestra capacidad de control, esta ventana de tiempo es lo suficientemente larga, podemos sondear", dijo Hu. "Ahora, con este aparato, podemos pensar en esto. Sin esta técnica, sin este papel, ni siquiera podemos pensar en esto".
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.