Misterio ultracongelado resuelto
Al manipular las moléculas de ultrafrío en medio de una reacción química, los investigadores descifran un acto de desaparición molecular
Anuncios
En una famosa parábola, tres ciegos se encuentran con un elefante por primera vez. Cada uno toca una parte - la trompa, la oreja o el costado - y concluye que la criatura es una gruesa serpiente, un abanico o una pared. Este elefante, dijo Kang-Kuen Ni, es como el mundo cuántico. Los científicos sólo pueden explorar una célula de esta vasta y desconocida criatura a la vez. Ahora, Ni ha revelado algunas más para explorar.
Todo comenzó el pasado diciembre, cuando ella y su equipo completaron un nuevo aparato que podía lograr las reacciones químicas a más baja temperatura de cualquier tecnología disponible actualmente y luego rompió y formó los enlaces más fríos en la historia del acoplamiento molecular. Pero sus reacciones ultracongeladas también ralentizaron inesperadamente la reacción a una velocidad lenta, regalando a los investigadores un vistazo en tiempo real de lo que ocurre durante una transformación química. Ahora, aunque se considera que las reacciones son demasiado rápidas para medirlas, Ni no sólo determinó la duración de esa reacción, sino que resolvió un misterio de ultracongelamiento en el proceso.
Con la química ultra-fría, Ni, la profesora asociada de Morris Kahn de química y biología química y de física, y su equipo enfriaron dos moléculas de potasio-rubidio hasta justo por encima del cero absoluto y encontraron el "intermedio", el espacio donde los reactantes se transforman en productos, que vivió durante unos 360 nanosegundos (todavía mil millonésimas de segundo, pero el tiempo suficiente). "No es el reactivo. No es el producto. Es algo intermedio", dijo Ni. Observar esa transformación, como tocar el costado de un elefante, puede decirle algo nuevo sobre cómo funcionan las moléculas, la base de todo.
Pero no se limitaron a observar.
"Esta cosa vive tanto tiempo que ahora podemos jugar con ella... con la luz", dijo Yu Liu, un estudiante graduado en la Escuela de Artes y Ciencias y primer autor de su estudio publicado en Física de la Naturaleza. "Los complejos típicos, como los de una reacción a temperatura ambiente, con los que no se podría hacer mucho porque se disocian en productos tan rápidamente."
Como los haces tractores de Star Trek, los láseres pueden atrapar y manipular las moléculas. En la física ultrafría, este es el método para capturar y controlar átomos, observarlos en su estado cuántico terrestre o forzarlos a reaccionar. Pero cuando los científicos pasaron de manipular átomos a meterse con moléculas, algo extraño sucedió: las moléculas comenzaron a desaparecer de la vista.
"Prepararon estas moléculas, con la esperanza de realizar muchas de las aplicaciones que prometían, por ejemplo, construir computadoras cuánticas, pero en cambio lo que ven es una pérdida", dijo Liu.
Los átomos alcalinos, como el potasio y el rubidio Ni y su equipo de estudio, son fáciles de enfriar en el reino ultracongelado. En 1997, los científicos ganaron el Premio Nobel de Física por enfriar y atrapar átomos alcalinos en la luz láser. Pero las moléculas son más débiles que los átomos: No son sólo una cosa esférica sentada ahí, dijo Liu, pueden rotar y vibrar. Al quedar atrapadas en la luz láser, las moléculas de gas chocaron entre sí como se esperaba, pero algunas simplemente desaparecieron.
Los científicos especularon que la pérdida molecular fue el resultado de las reacciones: dos moléculas chocaron entre sí y, en lugar de dirigirse en diferentes direcciones, se transformaron en nuevas especies. ¿Pero cómo?
"Lo que encontramos en este documento responde a esa pregunta", dijo Liu. "Lo que se usa para confinar la molécula es matar la molécula". En otras palabras, es culpa de la luz.
Cuando Liu y Ni usaron láseres para manipular ese complejo intermedio, en medio de su reacción química, descubrieron que la luz forzaba a las moléculas a salirse de su camino de reacción típico y a entrar en uno nuevo. Un par de moléculas, pegadas como un complejo intermedio, pueden "foto-excitarse" en lugar de seguir su camino tradicional, dijo Liu. Las moléculas alcalinas son particularmente susceptibles debido al tiempo que viven en su complejo intermedio.
"Básicamente, si quieres eliminar la pérdida", dijo Liu, "tienes que apagar la luz. Tienes que encontrar otra forma de atrapar estas cosas". Los imanes, por ejemplo, o los campos eléctricos también pueden atrapar moléculas. "Pero todo esto es técnicamente exigente", dijo Liu. La luz es simplemente más simple.
A continuación, Ni quiere ver a dónde van estos complejos cuando desaparecen. Ciertas longitudes de onda de la luz (como el infrarrojo que el equipo usó para excitar sus moléculas de potasio-rubidio) pueden crear diferentes caminos de reacción, pero nadie sabe qué longitudes de onda envían moléculas a qué nuevas formaciones.
También planean explorar cómo se ve el complejo en varias etapas de transformación. "Para probar su estructura", dijo Liu, "podemos variar la frecuencia de la luz y ver cómo varía el grado de excitación". A partir de ahí, podemos averiguar dónde están los niveles de energía de esta cosa, lo que informa sobre su construcción mecánica cuántica".
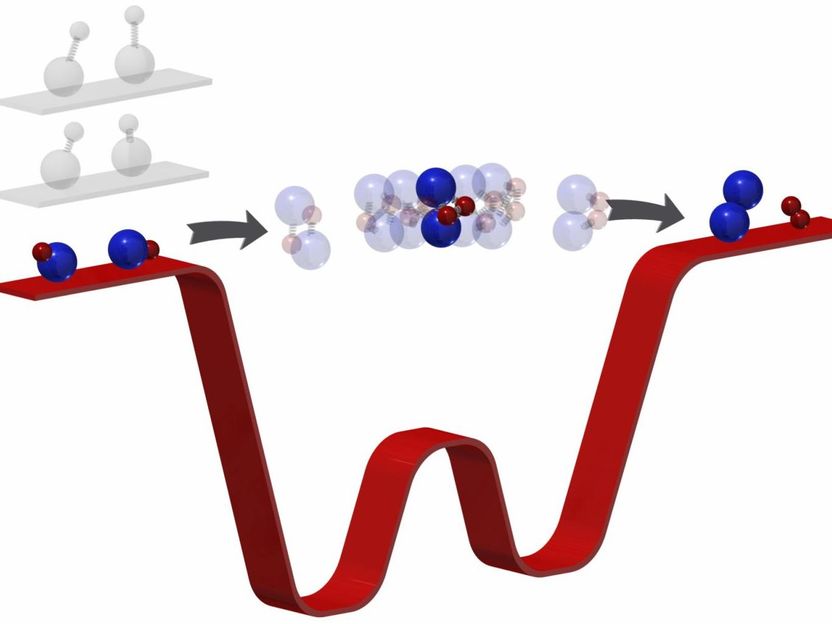
Los investigadores de Harvard descubren que las temperaturas ultracongeladas ralentizan las reacciones químicas a velocidades lentas, dándoles un vistazo de cómo las moléculas se transforman y de cómo se puede comprender el mundo cuántico.
Ni Lab/Harvard University
"Esperamos que esto sirva como un sistema modelo", dijo Ni, un ejemplo de cómo los investigadores pueden explorar otras reacciones a baja temperatura que no involucren al potasio y al rubidio.
"Esta reacción es, como muchas otras reacciones químicas, una especie de universo en sí mismo", dijo Liu. Con cada nueva observación, el equipo revela un pequeño trozo del elefante cuántico gigante. Dado que hay un número infinito de reacciones químicas en el universo conocido, todavía hay un largo, largo camino por recorrer.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática.
Anuncios










































