Un catalizador de 40 años revela sus secretos
Los hallazgos ayudarán a que la investigación catalizadora dé un importante paso adelante
Anuncios
La "Silicalita de titanio-1" (TS-1) no es un catalizador nuevo: han pasado casi 40 años desde su desarrollo y el descubrimiento de su capacidad para convertir el propileno en óxido de propileno, un importante producto químico básico de la industria química. Ahora, mediante la combinación de varios métodos, un equipo de científicos del ETH de Zurich, la Universidad de Colonia, el Instituto Fritz Haber y BASF ha desvelado el sorprendente mecanismo de acción de este catalizador. Estos hallazgos ayudarán a la investigación del catalizador a dar un importante paso adelante.
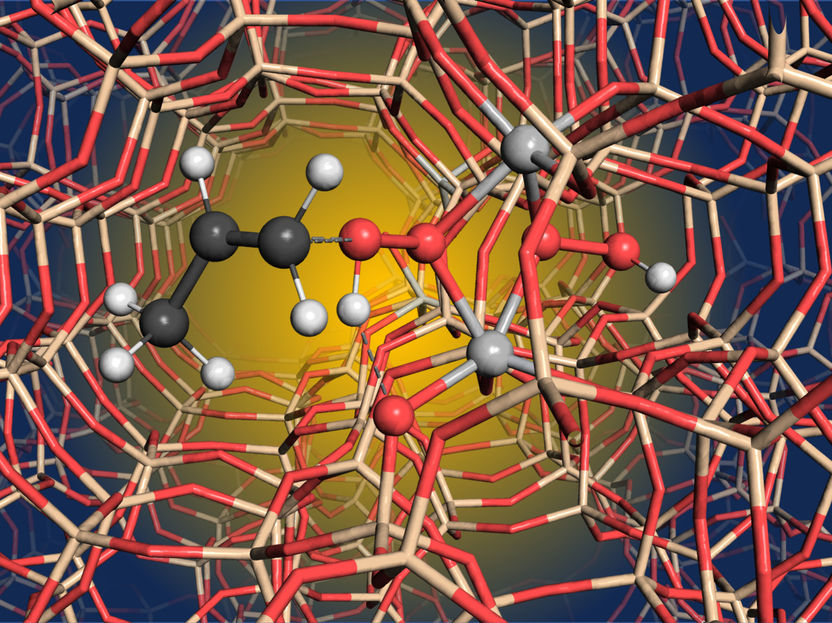
Modelo 3D del centro activo del catalizador Titanium Silicalite-1 con el par de titanio (gris claro)
ETH Zürich
El óxido de propileno se utiliza en la industria para fabricar productos como poliuretanos, aditivos anticongelantes y fluidos hidráulicos. Más de 11 millones de toneladas métricas de óxido de propileno se producen anualmente en la industria química en todo el mundo, de las cuales 1 millón de toneladas métricas ya se producen por la oxidación del propileno con peróxido de hidrógeno. Esta reacción química es catalizada por el TS-1, un material microporoso y cristalino compuesto de silicio y oxígeno y que contiene pequeñas cantidades de titanio. El catalizador se ha utilizado con éxito durante 40 años y los expertos asumieron que el centro activo en TS-1 contiene átomos de titanio individuales y aislados que aseguran la reactividad especial del catalizador.
Un equipo de investigadores del ETH Zurich, la Universidad de Colonia, el Instituto Fritz Haber y BASF cuestionaron esta suposición. "En los últimos años, han surgido dudas sobre si la suposición sobre el mecanismo de acción es correcta, ya que se basa principalmente en analogías con catalizadores comparables y menos en pruebas experimentales. Pero si tratas de optimizar un catalizador sobre la base de una suposición errónea, es muy difícil y puede llevarte en la dirección completamente equivocada. Por lo tanto, era importante examinar esta suposición más de cerca", explica el científico de BASF Dr. Henrique Teles, uno de los coautores de la publicación científica, el punto de partida de la colaboración.
En un estudio que ahora se publica en "Nature", el equipo fue capaz, mediante el uso de estudios de RMN de estado sólido y de modelos informáticos, de demostrar que dos átomos de titanio vecinos son necesarios para explicar la actividad catalítica particular. Esto a su vez llevó al equipo de investigación a concluir que los átomos de titanio no están aislados, sino que el centro catalíticamente activo consiste en un par de titanio. "Ninguno de los métodos que utilizamos en el estudio son fundamentalmente nuevos, pero ninguno de los grupos de investigación que participan en el estudio podría haber llevado a cabo la investigación por su cuenta", subraya el profesor Christophe Copéret de ETH Zurich, el autor por correspondencia de la publicación. "Sólo la combinación de diferentes campos de especialización y diversas técnicas permitieron examinar más de cerca el centro activo del catalizador".
"Hemos trabajado durante muchos años para dilucidar el mecanismo de reacción de un catalizador de titanio homogéneo y hemos descubierto que, contrariamente a las suposiciones de la literatura, el peróxido de hidrógeno es activado por un par de titanio. Fue realmente un momento especial cuando vimos en el estudio actual que los hallazgos de la catálisis homogénea también se aplican a la catálisis heterogénea", dijo el coautor, Prof. Albrecht Berkessel de la Universidad de Colonia. Y el Dr. Thomas Lunkenbein, co-autor del Instituto Fritz Haber de Berlín, añade: "Estamos muy contentos de haber podido hacer una contribución a este estudio. Con nuestros análisis, fuimos capaces de corroborar las conclusiones. El conocimiento de un centro activo diatómico es de fundamental importancia y abre nuevas posibilidades en la investigación de catalizadores".
El equipo está convencido de que los resultados de este estudio no sólo ayudarán a mejorar los catalizadores existentes, sino también a desarrollar nuevos catalizadores homogéneos y heterogéneos.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.










































