El hierro oxidado puede ser su peor enemigo
Las simulaciones muestran que el hierro cataliza la corrosión en el dióxido de carbono "inerte
Anuncios
El hierro que se oxida en el agua teóricamente no debería corroerse en contacto con un fluido supercrítico "inerte" de dióxido de carbono. Pero lo hace.
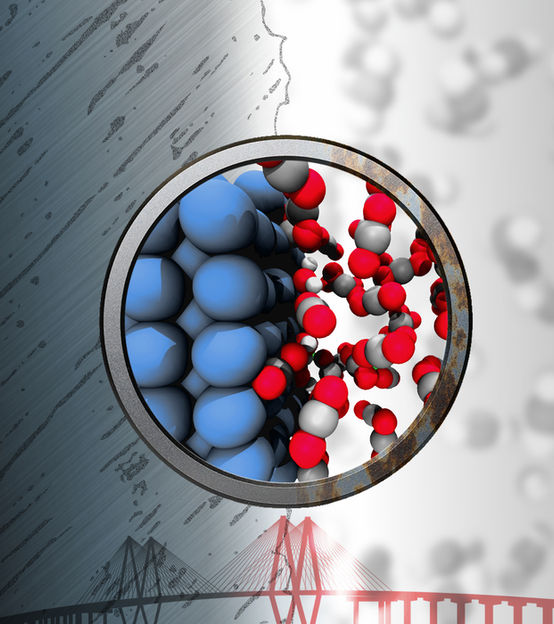
El hierro (azul) puede reaccionar con trazas de agua para producir sustancias químicas corrosivas a pesar de estar bañado en fluidos supercríticos "inertes" de dióxido de carbono. Las simulaciones atomísticas realizadas en la Universidad de Rice muestran cómo se produce esta reacción.
Illustration by Evgeni Penev/Rice University
La razón ha eludido a los científicos de materiales hasta ahora, pero un equipo de la Universidad de Rice tiene una teoría que podría contribuir a nuevas estrategias para proteger el hierro del medio ambiente.
El teórico de materiales Boris Yakobson y sus colegas de la Escuela de Ingeniería George R. Brown de Rice descubrieron, mediante simulaciones a nivel atómico, que el propio hierro desempeña un papel en su propia corrosión cuando se expone aCO2 supercrítico (sCO2) y a trazas de agua, al promover la formación de especies reactivas en el fluido que vuelven a atacarlo.
En su investigación, publicada en la revista Matter de Cell Press, concluyen que podrían emplearse finas capas hidrofóbicas de materiales 2D como el grafeno o el nitruro de boro hexagonal como barrera entre los átomos de hierro y los elementos reactivos del sCO2.
El estudiante de posgrado de Rice Qin-Kun Li y el investigador Alex Kutana son coautores del artículo. El profesor asistente de investigación de Rice, Evgeni Penev, es coautor.
Los fluidos supercríticos son materiales que se encuentran a una temperatura y presión que los mantiene más o menos entre fases, es decir, no son totalmente líquidos, pero tampoco son totalmente gaseosos. Las propiedades del sCO2 lo convierten en un fluido de trabajo ideal porque, según los investigadores, es "esencialmente inerte", no corrosivo y de bajo coste.
"Eliminar la corrosión es un reto constante, y está en la mente de mucha gente ahora que el gobierno se prepara para invertir fuertemente en infraestructuras", dijo Yakobson, catedrático de Ciencia de los Materiales y Nanoingeniería Karl F. Hasselmann y profesor de química. "El hierro es un pilar de las infraestructuras desde la antigüedad, pero sólo ahora somos capaces de obtener una comprensión atomística de cómo se corroe".
Las simulaciones del laboratorio Rice revelan que el diablo está en los detalles. Estudios anteriores han atribuido la corrosión a la presencia de agua en masa y otros contaminantes en el superfluido, pero no es necesariamente así, dijo Yakobson.
"El agua, como impureza principal en el sCO2, proporciona una red de enlaces de hidrógeno para desencadenar reacciones interfaciales conel CO2 y otras impurezas como el óxido nitroso y formar ácido corrosivo perjudicial para el hierro", dijo Li.
Las simulaciones también mostraron que el propio hierro actúa como catalizador, reduciendo las barreras de energía de reacción en la interfaz entre el hierro y el sCO2, lo que finalmente conduce a la formación de una serie de especies corrosivas: oxígeno, hidróxido, ácido carboxílico y ácido nitroso.
Para los investigadores, el estudio ilustra el poder de la modelización teórica para resolver complicados problemas de química, en este caso prediciendo reacciones termodinámicas y estimaciones de las tasas de corrosión en la interfaz entre el hierro y el sCO2. También demostraron que todas las apuestas se cancelan si hay más que un rastro de agua en el superfluido, lo que acelera la corrosión.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.