El elemento más pesado jamás estudiado químicamente
Los experimentos logran determinar las propiedades del moscovio y el nihonio
Anuncios
Un equipo internacional dirigido por científicos del GSI/FAIR de Darmstadt, la Universidad Johannes Gutenberg de Maguncia y el Instituto Helmholtz de Maguncia ha logrado determinar las propiedades químicas de los elementos superpesados moscovio y nihonio (elementos 115 y 113) producidos artificialmente. El moscovio se convierte así en el elemento más pesado jamás estudiado químicamente. Ambos elementos recién caracterizados son químicamente más reactivos que el flerovio (elemento 114), estudiado anteriormente en el GSI/FAIR. Los resultados se publican en la revista Frontiers in Chemistry.
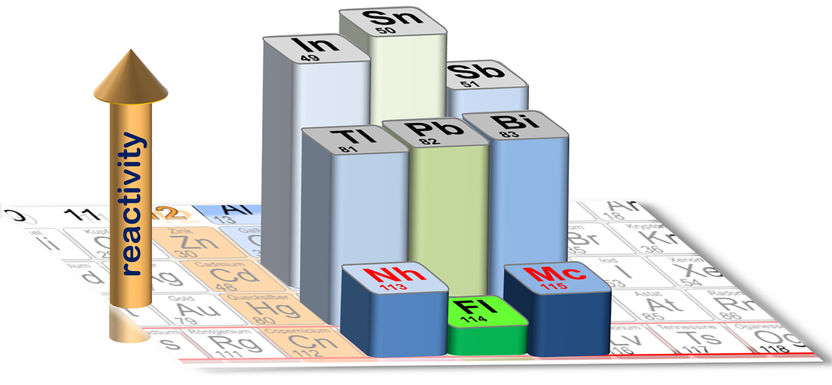
Recorte de la tabla periódica: La altura de las barras de los elementos resaltados representa la fuerza de la unión sobre una superficie de cuarzo.
A. Yakushev/Ch.E. Düllmann
Con este resultado, los experimentos del GSI/FAIR proporcionan ahora datos sobre los tres elementos superpesados 113, 114 y 115, lo que permite una clasificación fiable de sus propiedades y una evaluación de la estructura de la tabla periódica en esta región extrema. A medida que los elementos se hacen más pesados, sus numerosos protones en el núcleo aceleran los electrones que giran alrededor del núcleo a velocidades cada vez mayores, tan altas que entran en acción efectos sólo explicables con la famosa teoría de la relatividad de Einstein. La velocidad hace que los electrones sean más pesados.
En el plomo (elemento 82), por ejemplo, los efectos de estos procesos ya están actuando y contribuyen a los procesos químicos de las baterías de plomo. Los vecinos de la izquierda y la derecha, el talio y el bismuto, se comportan de forma diferente. El efecto, aunque pequeño, se localiza en el plomo. ¿Podría un elemento superpesado ser una alternativa al plomo? ¿Qué le parece el vecino más pesado del grupo inferior de la tabla periódica, el flerovio, elemento 114, descubierto y estudiado químicamente sólo en los últimos 20 años? Se ha descubierto que es muy distinto del plomo, se transforma en gas con facilidad y es menos reactivo químicamente.
Para encontrar respuestas, era necesario probar también los dos elementos vecinos, el 113, nihonio, y el 115, moscovio. Aunque ya se habían dado las primeras pistas sobre la química del nihonio, hasta ahora nadie había logrado estudiar la química del moscovio, cuyo isótopo más adecuado sólo existe durante unas 20 centésimas de segundo.
Ahora, la colaboración internacional del GSI Helmholtzzentrum für Schwerionenforschung de Darmstadt (Alemania) ha logrado esta hazaña. El equipo informó de que ambos vecinos, tanto el nihonio como el moscovio, muestran una reactividad química mayor que el flerovio intermedio. El efecto local observado en el plomo también se aprecia en el flerovio, aunque con mucha más intensidad, lo que no es de extrañar dada su carga nuclear mucho mayor.
La observación de apenas un puñado de átomos fue suficiente para obtener este resultado. Sin embargo, fueron necesarios dos meses de trabajo ininterrumpido en el acelerador de iones pesados del GSI/FAIR para lograrlo. Para producir los elementos superpesados, el equipo irradió finas láminas que contenían americio-243 (elemento 95), en sí mismo un elemento artificial, con intensos haces de iones de calcio-48 (elemento 20). Su fusión dio lugar a núcleos de moscovio-288 (elemento 115), que se transformaron en una fracción de segundo en nihonio-284 (elemento 113).
Un gas inerte hizo fluir ambos elementos a través de un conjunto de detectores cubiertos con una fina capa de cuarzo. Los detectores registran la desintegración de cada uno de los átomos superpesados y determinan si los átomos forman un enlace químico con el cuarzo lo suficientemente fuerte como para retenerlos donde se encuentran por primera vez con la superficie. Una unión más débil da lugar a un mayor transporte por el gas. De este modo, el patrón registrado en el conjunto de detectores proporciona información sobre la fuerza de los enlaces químicos y, por tanto, sobre la reactividad química de los elementos. Los elementos de baja reactividad podrían incluso salir del conjunto, pero sólo para encontrarse con detectores cubiertos de oro. Los enlaces con el oro suelen ser más fuertes que con el cuarzo, lo que garantiza que cada átomo estudiado quede retenido y registrado.
"Gracias a una nueva configuración para la separación y detección química en combinación con el separador electromagnético TASCA, nuestros estudios de cromatografía de gases han podido ampliarse a elementos químicos más reactivos como el nihonio y el moscovio", explica el Dr. Alexander Yakushev de GSI/FAIR, portavoz de la colaboración internacional. "Hemos conseguido aumentar la eficacia y reducir el tiempo necesario para la separación química hasta tal punto que hemos podido observar el moscovio-288, de vida muy corta, y a un ritmo aún mayor, de unos dos átomos detectados cada semana, su hija el nihonio-284".
En total, se registraron cuatro átomos de moscovio, todos en el conjunto cubierto de cuarzo. Entre los 14 átomos de nihonio detectados, se observó una deposición mayoritaria sobre el cuarzo, lo que apunta a la formación de un enlace químico. Un átomo alcanzó el conjunto cubierto de oro, lo que indica que el enlace con el cuarzo no es muy fuerte. Esto contrasta con el comportamiento de los homólogos más ligeros, el talio (para el nihonio) y el bismuto (para el moscovio), de los que se sabe que forman enlaces fuertes con el cuarzo. Del mismo modo, el plomo, el homólogo del flerovio, forma enlaces fuertes con el cuarzo, mientras que el flerovio no.
El conjunto completo de datos sobre estos elementos muestra que los elementos superpesados son mucho menos reactivos que sus homólogos más ligeros, lo que se atribuye a la inercia asociada a la aparición de efectos relativistas. El efecto más pronunciado se observa localmente en el flerovio, que sigue siendo un metal, pero muy poco reactivo, un comportamiento que indica la presencia de (sub)envolturas electrónicas cerradas, casi como en los gases nobles no reactivos. Los resultados demuestran la influencia de la teoría de la relatividad de Einstein en la tabla periódica y, al mismo tiempo, establecen un nuevo récord para el elemento más pesado jamás estudiado químicamente.
Con los avances tecnológicos surgen nuevas necesidades de materiales. ¿Podrían contribuir a ello nuevos elementos? Al igual que los coches pasan de funcionar con combustibles fósiles a hacerlo con electricidad, también otros elementos de nuestra vida cotidiana van desapareciendo, siendo sustituidos por tecnología basada en materiales novedosos. El primer dispositivo basado en flerovio aún no está a la vuelta de la esquina. Actualmente sólo se pueden producir átomos individuales por semana, que duran menos de un segundo. A medida que avance la tecnología, esto podría cambiar y, con el tiempo, se podría disponer de mayores cantidades. No sabemos si podrían servir en futuras baterías, como agentes médicos, o enriquecer nuestras vidas de formas hoy inconcebibles. Pero gracias a los innovadores experimentos de Darmstadt, los futuros investigadores tendrán una ventaja y ya conocerán el carácter químico de estos nuevos materiales. El resultado también abre nuevas perspectivas para la instalación internacional FAIR (Facility for Antiproton and Ion Research), actualmente en construcción en Darmstadt.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.
Publicación original
A. Yakushev, J. Khuyagbaatar, Ch. E. Düllmann, M. Block, R. A. Cantemir, D. M. Cox, D. Dietzel, F. Giacoppo, Y. Hrabar, M. Iliaš, E. Jäger, J. Krier, ... L. G. Sarmiento, B. Schausten, U. Scherer, P. Thörle-Pospiech, N. Trautmann, M. Wegrzecki, P. Wieczorek; "Manifestation of relativistic effects in the chemical properties of nihonium and moscovium revealed by gas chromatography studies"; Frontiers in Chemistry, Volume 12, 2024-9-23