Mecanismo de itinerancia revelado en bromoformo
Un experimento demuestra la existencia de un mecanismo de itinerancia en reacciones fotoquímicas largamente debatido
Anuncios
El compuesto halometano bromoformo (CHBr3) tiene efectos devastadores sobre la capa de ozono. En las capas superiores de la atmósfera, el bromoformo reacciona con la radiación UV, liberando moléculas de bromo que destruyen las moléculas de ozono. Esta reacción, sin embargo, ha desconcertado durante mucho tiempo a los científicos; las moléculas implicadas parecen vagar unas respecto a otras de una forma que energéticamente no tiene sentido. Los científicos del XFEL europeo han hallado por primera vez pruebas estructurales de este mecanismo de vagabundeo, que lo convierten en una característica universal de las reacciones fotoquímicas. El estudio, publicado en Nature Communications, aporta datos clave para el campo de la fotoquímica atmosférica y el impacto de compuestos halometánicos como el bromoformo en la capa de ozono.
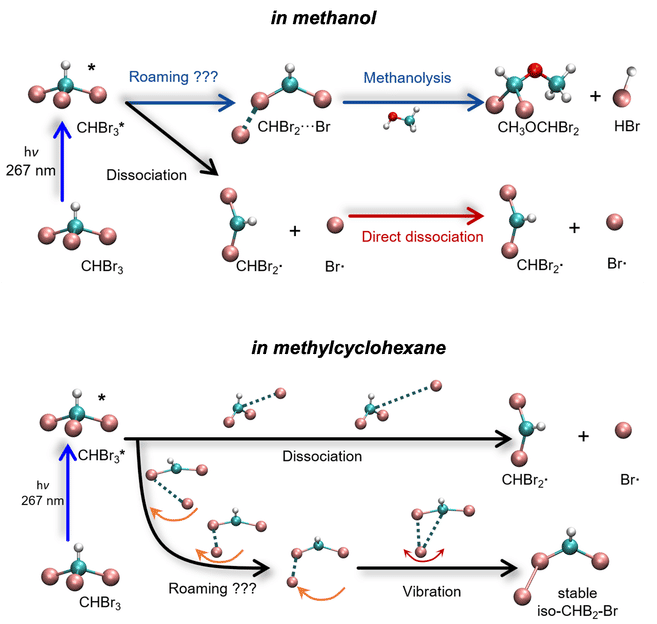
Pie de foto: Dinámica de reacción recién elucidada del bromoformo (CHBrâ'ƒ) en los disolventes metanol (arriba) y metilciclohexano (abajo). Los átomos se representan de la siguiente manera: carbono (cian), bromo (rosa), hidrógeno (gris) y oxígeno (rojo).
European XFEL
La capa de ozono envuelve la Tierra a unos 15-30 km por encima de la superficie del planeta. El gas ozono absorbe la luz ultravioleta cuando entra en la atmósfera, protegiendo así la vida en la Tierra de los efectos de la radiación nociva. Sin embargo, el ozono reacciona fácilmente con otros compuestos que también se encuentran en la estratosfera, lo que provoca su agotamiento y, en última instancia, la creación del agujero de ozono. Uno de estos compuestos es el bromoformo (CHBr3). Emitido por la vida marina, como el fitoplancton y las algas, este compuesto halometano interactúa con la luz ultravioleta cuando asciende a las capas superiores de la atmósfera, suspendido en gotas de agua o aerosoles. La interacción con la luz ultravioleta desencadena una reacción que acaba liberando moléculas de bromo. Más de 100 veces más destructivo que otros gases halógenos como el cloro, el bromo es extremadamente reactivo y destruye rápidamente las moléculas de ozono. Este tipo de fotorreacciones son las causantes del agujero de ozono. Ahora, utilizando el XFEL europeo, los científicos han revelado detalles estructurales clave de este tipo de reacción, mejorando nuestra comprensión de la química atmosférica.
El rompecabezas de las moléculas errantes
Los detalles de la reacción ultrarrápida inducida por la luz en la que interviene el bromoformo han desconcertado a los científicos durante mucho tiempo. Se sabe que tras la interacción inicial con la luz ultravioleta, el bromoformo se rompe en fragmentos, algunos de los cuales se realinean para formar compuestos químicos estables. Sin embargo, curiosamente, las moléculas implicadas en estas reacciones no se comportan como cabría esperar. "Tras la fragmentación del bromoformo por la luz ultravioleta se acaban formando complejos intermedios estables", explica Qingyu Kong, científico del sincrotrón Soleil y principal científico del estudio. "Sin embargo, en las etapas iniciales de la reacción estos fragmentos pueden unirse en configuraciones estructurales que no parecen tener sentido desde el punto de vista energético, al menos desde la perspectiva clásica. En lugar de separarse completamente o unirse de un modo que consuma la menor cantidad de energía, los fragmentos migran lentamente unos respecto a otros de un modo que elude los estados de transición convencionales." Para explicar estas observaciones, los científicos postularon la hipótesis denominada itinerancia, que indica la forma en que los iones parecen vagar más lejos para encontrar una nueva configuración estable. Sin embargo, hasta la fecha no se han aportado pruebas estructurales directas que respalden esta teoría en el bromoformo.
Gracias al XFEL europeo, un equipo de investigadores ha resuelto por primera vez este mecanismo de vagabundeo ultrarrápido. Estudios anteriores realizados en sincrotrones habían revelado los productos finales de estas reacciones, pero no habían sido capaces de desentrañar los pasos iniciales. "Era evidente que el primer paso crucial de la reacción, donde se cree que tiene lugar el mecanismo de itinerancia, se produce mucho más rápido de lo que los pulsos de rayos X del sincrotrón podían detectar", explica Dmitry Khakhulin, científico del XFEL europeo y autor principal del reciente estudio.
Pulsos de femtosegundo
Para su experimento, los científicos inyectaron soluciones de bromoformo en forma de finos chorros en la zona de experimentación del instrumento FXE del XFEL Europeo. Un pulso de láser óptico de femtosegundo desencadenó la reacción; a continuación se utilizó un pulso de rayos X retardado para captar información sobre las distintas etapas de la reacción. El método se conoce como dispersión de rayos X en solución resuelta en el tiempo en femtosegundos.
A diferencia de experimentos anteriores, los pulsos ultracortos de rayos X generados por el XFEL europeo permitieron a los científicos captar ahora todos los pasos estructurales de la reacción, desde la ruptura de los primeros enlaces y la dinámica de itinerancia de los fragmentos hasta la formación de bromo y diversos productos de recombinación. Los resultados mostraron que en los 150 femtosegundos siguientes al inicio de la reacción se había producido la itinerancia y los compuestos intermedios estables comenzaban a formarse gradualmente.
"Gracias a los pulsos ultracortos de rayos X generados por el XFEL europeo, pudimos aportar por primera vez pruebas estructurales de la itinerancia en el bromoformo", afirma Khakhulin.
Influencia del disolvente
Estudios anteriores en sincrotrones también indicaban que el resultado de la reacción estaba influido por el disolvente. Para sus estudios en el XFEL europeo, los científicos utilizaron dos líquidos diferentes como disolventes -metanol y metilciclohexano- para determinar si éste era el caso.
"Nuestros resultados mostraron que, aunque el intermediario se formaba en ambos líquidos, lo que sucedía después dependía en gran medida del disolvente en el que se suspendía el bromoformo", explica Kong. Cuando se suspendía en metanol, las moléculas de metanol competían por unirse al compuesto intermedio, de modo que el intermedio inicial de corta vida se descomponía. Sin embargo, el metilciclohexano, menos reactivo, hizo que el intermedio se relajara hasta convertirse en un producto estable.
"En conjunto, estos nuevos conocimientos son pasos importantes hacia una comprensión más completa de la fotoquímica atmosférica y ofrecen un nuevo marco para entender el comportamiento de compuestos como el bromoformo en el contexto del medio ambiente en fase gaseosa, los aerosoles y las gotas de agua", concluye Kong.
Este estudio se realizó en el marco de una colaboración a largo plazo en el instrumento FXE. El trabajo implicó una estrecha colaboración entre el XFEL europeo, el sincrotrón Soleil, la Universidad ShanghaiTech y el ESRF.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.
Publicación original
Peiyuan Su, Jihao Zhang, Hao Wang, Yifeng Jiang, Sharmistha Paul Dutta, Mengxu Li, Hazem Yousef, Peter Zalden, Kai Zhang, Ruixue Zhu, Xuan Liu, Yingqi Wang, Sophie E. Canton, Diana Bregenholt Jakobsen, Doriana Vinci, Wenkai Zhang, Jinggang Lan, Tsu-Chien Weng, Wenge Yang, Michael Wulff, Christopher Milne, Dmitry Khakhulin, Qingyu Kong; "Ultrafast solvent-modulated roaming mechanism in bromoform revealed by femtosecond X-ray solution scattering"; Nature Communications, Volume 17, 2026-2-9
















































