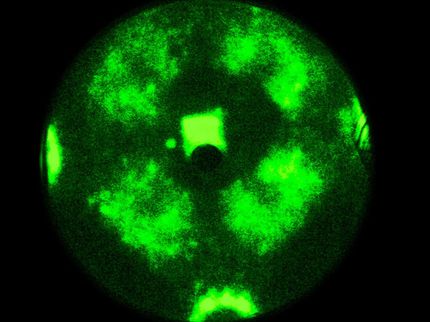
Caos a escala nanométrica
Investigación del caos aplicada a la nanoquímica
Anuncios
A veces, las reacciones químicas no se desarrollan únicamente de forma estacionaria en una dirección, sino que muestran oscilaciones espaciotemporales. En la TU Wien se ha observado ahora una transición a un comportamiento caótico a escala nanométrica.
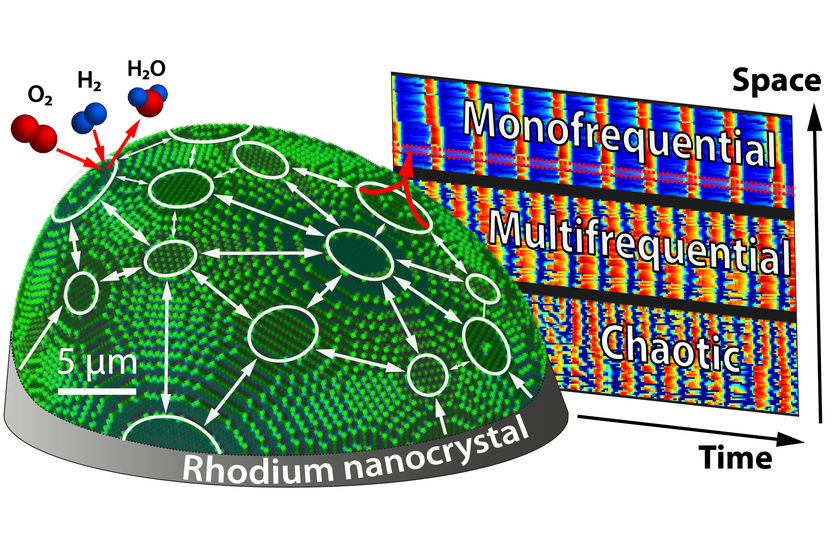
Nanochaos en un nanocristal de rodio asimétrico
TU Wien
El comportamiento caótico se conoce normalmente en sistemas grandes: por ejemplo, en el clima, en asteroides en el espacio que son atraídos simultáneamente por varios cuerpos celestes grandes o en péndulos oscilantes acoplados entre sí. A escala atómica, sin embargo, no se suele encontrar el caos: predominan otros efectos. Ahora, por primera vez, científicos de la Universidad Técnica de Viena han podido detectar indicios claros de caos a escala nanométrica, en reacciones químicas en diminutos cristales de rodio. Los resultados se han publicado en la revista Nature Communications.
De inactiva a activa, y viceversa
La reacción química estudiada es en realidad bastante sencilla: con la ayuda de un catalizador de metal precioso, el oxígeno reacciona con el hidrógeno para formar agua, que es también el principio básico de una pila de combustible. La velocidad de reacción depende de las condiciones externas (presión, temperatura). En determinadas condiciones, sin embargo, esta reacción muestra un comportamiento oscilante, aunque las condiciones externas sean constantes. "De forma similar a como un péndulo oscila de izquierda a derecha y viceversa, la velocidad de reacción oscila entre apenas perceptible y elevada y, por tanto, el sistema catalítico oscila de un lado a otro entre estados inactivos y activos", explica el profesor Günther Rupprechter, del Instituto de Química de Materiales de la Universidad Técnica de Viena.
Un péndulo es un ejemplo clásico de algo predecible: si lo perturbas un poco o lo pones en movimiento dos veces de formas ligeramente distintas, se comporta en líneas generales igual. En este sentido, es lo contrario de un sistema caótico, en el que diferencias mínimas en las condiciones iniciales conducen a resultados muy distintos en el comportamiento a largo plazo. Un buen ejemplo de este comportamiento son varios péndulos conectados por bandas elásticas.
Establecer exactamente las mismas condiciones iniciales dos veces es imposible
"En principio, por supuesto, las leyes de la naturaleza siguen determinando exactamente cómo se comportan los péndulos", afirma el profesor Yuri Suchorski (TU Wien). "Si pudiéramos poner en marcha un sistema de péndulos acoplados de este tipo exactamente de la misma manera dos veces, los péndulos se moverían exactamente igual las dos veces". Pero en la práctica, eso es imposible: nunca podrás recrear perfectamente la misma situación inicial la segunda vez que lo hiciste la primera - e incluso una diferencia insignificante en las condiciones iniciales hará que el sistema se comporte de forma completamente diferente a la primera vez - este es el famoso "efecto mariposa": pequeñas diferencias en las condiciones iniciales conducen a enormes diferencias en el estado en un momento posterior.
Ahora se ha observado algo muy parecido durante las oscilaciones químicas en un nanocristal de rodio: "El cristal consta de muchas nanofacies de superficie diferentes, como un diamante pulido, pero mucho más pequeñas, del orden de nanómetros", explican Maximilian Raab y Johannes Zeininger, que realizaron los experimentos. "En cada una de estas facetas, la reacción química oscila, pero las reacciones en las facetas vecinas están acopladas".
Pasar del orden al caos
El comportamiento de acoplamiento puede controlarse ahora de una forma extraordinaria: cambiando la cantidad de hidrógeno. Al principio, una faceta domina y marca el ritmo como un marcapasos. Todas las demás facetas se unen y oscilan al mismo ritmo. Si se aumenta la concentración de hidrógeno, la situación se complica. Las distintas facetas oscilan con frecuencias diferentes, pero su comportamiento sigue siendo periódico y predecible. Sin embargo, si se aumenta aún más la concentración de hidrógeno, este orden se rompe de repente. El caos gana, las oscilaciones se vuelven impredecibles, pequeñas diferencias en la situación inicial conducen a patrones de oscilación completamente diferentes - una clara señal de caos.
"Esto es sorprendente, porque no cabría esperar un comportamiento caótico en estructuras de tamaño nanométrico", explica Yuri Suchorski. "Cuanto más pequeño es el sistema, mayor es la contribución del ruido estocástico. De hecho, el ruido, que es algo completamente distinto del caos, debería dominar el comportamiento del sistema: es aún más interesante que haya sido posible "extraer" indicios de caos". Resultó especialmente útil un modelo teórico desarrollado por el profesor Keita Tokuda (Universidad de Tsukuba).
Investigación del caos aplicada a la nanoquímica
"Hace décadas que se investiga la teoría del caos, y ya se ha aplicado con éxito a reacciones químicas en sistemas más grandes (macroscópicos), pero nuestro estudio es el primer intento de trasladar los amplios conocimientos de este campo a la escala nanométrica", afirma Günther Rupprechter. "Pequeñas desviaciones en la simetría del cristal pueden determinar si el catalizador se comporta de forma ordenada y predecible o de forma desordenada y caótica. Esto es importante para distintas reacciones químicas, y quizá incluso para sistemas biológicos".
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.