Nuevas herramientas químicas para modificar y estudiar biomoléculas
Anuncios
Comprender la estructura y el metabolismo de las células y los organismos vivos es esencial para el desarrollo de nuevos fármacos y diagnósticos. La disponibilidad de herramientas químicas que permiten a los científicos editar biomoléculas, como las proteínas, con una resolución a nivel atómico, ha contribuido en gran medida al progreso de la biología química.
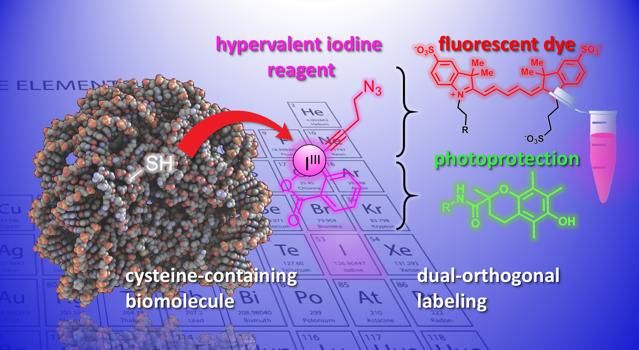
Una ilustración de la reacción química desarrollada en el estudio.
J. Waser/B. Fierz (EPFL)
Las proteínas son macromoléculas construidas a partir de un conjunto de veinte aminoácidos químicamente diferentes. Un enfoque clave para modificar las proteínas es reaccionar con el átomo de azufre en el aminoácido cisteína. Sin embargo, los métodos actuales siguen siendo problemáticos en términos de eficiencia, selectividad y estabilidad del producto final (el "aducto").
Ahora, los laboratorios de Jérôme Waser y Beat Fierz del Instituto de Ciencias Químicas e Ingeniería de la EPFL han desarrollado un nuevo método para modificar cisteínas en péptidos y proteínas. El método utiliza un grupo de moléculas orgánicas altamente reactivas, las etilbenziodoxolonas (EBX). Lo que hace que las EBX sean altamente reactivas es que contienen un átomo de yodo unido a tres grupos sustitutivos. Esta situación no natural conduce a una alta reactividad de estos reactivos llamados "yodo hipervalente".
Por primera vez, los investigadores pudieron generar un aducto simple de biomoléculas-EBX mientras mantenían su grupo reactivo de yodo en la molécula final. La reacción puede ser realizada fácilmente por un no experto bajo condiciones fisiológicas estándar.
El producto final son quimeras de reactivos de yodo hipervalentes que pueden actuar como puntos de unión duales para dos nuevos grupos químicos, abriendo nuevas oportunidades para el estudio de los procesos biológicos.
"Una nueva funcionalidad puede ser introducida a través de'click-chemistry', una reacción bien establecida en biología química", dice Waser. "Usando catalizadores de paladio, otra modificación selectiva puede ser lograda en el átomo reactivo de yodo, lo que llamaríamos una funcionalidad'biorthogonal', ya que no existe en la naturaleza". La introducción de estos grupos reactivos exóticos en las biomoléculas es actualmente una de las herramientas más importantes de la biología química, ya que permite el estudio de los procesos biológicos sin interferir con ellos.
Los científicos demostraron el potencial del método introduciendo un conjunto diverso de grupos químicos en las biomoléculas. Por ejemplo, los científicos usaron el mango doble para unir un tinte fluorescente y un grupo fotoprotector en un neuropéptido simultáneamente. Combinarlos mejora la fotoestabilidad del tinte y permite obtener imágenes de alta resolución de las interacciones moleculares con una sola molécula.
Más allá de los péptidos, modificaron aún más las pequeñas proteínas, e incluso los grandes complejos de proteínas-ADN, los llamados nucleosomas. A medida que los nucleosomas organizan el genoma, etiquetarlos con tintes fluorescentes puede ayudar a descifrar cómo la naturaleza regula la expresión génica.
"Lo que hemos desarrollado aquí es un nuevo método para modificar proteínas basado en estudios fundamentales de reactividad química", dice Fierz. "Ya lo hemos utilizado para modificar de histonas, y hemos realizado experimentos de fluorescencia en células vivas. Con estos ejemplos, hemos sentado las bases para una mejor comprensión de los procesos biológicos".
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.