Los químicos muestran que está de moda ser cuadrado
Sus azetidinas sintéticas podrían ayudar a simplificar el diseño de fármacos para enfermedades neurológicas
Anuncios
Los químicos de la Universidad de Rice quieren hacer un comentario: Los átomos de nitrógeno son para los cuadrados.
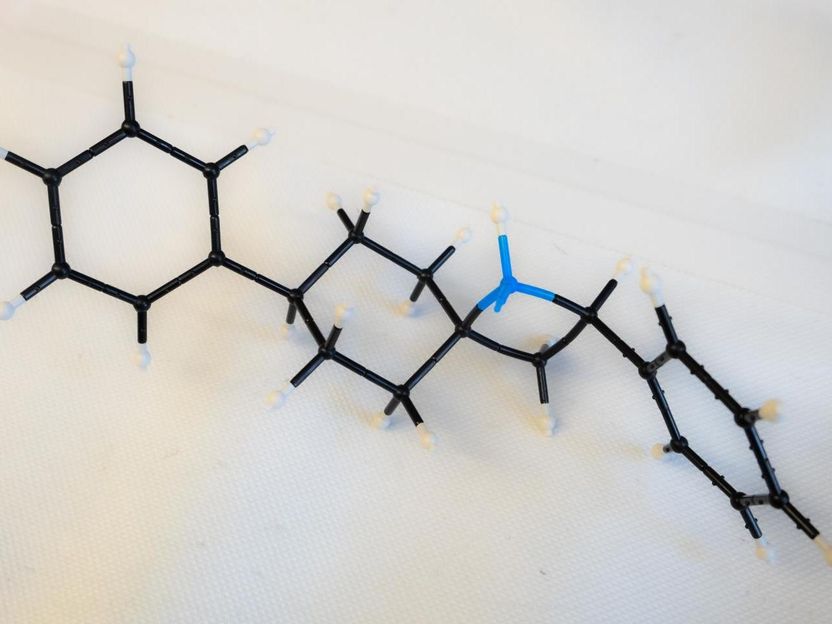
Un modelo muestra un nitrógeno azul expuesto en un anillo de cuatro miembros, la parte activa de una molécula de azetidina. Los científicos de la Universidad de Rice sintetizaron la molécula para simplificar el proceso de diseño del medicamento.
Jeff Fitlow/Rice University
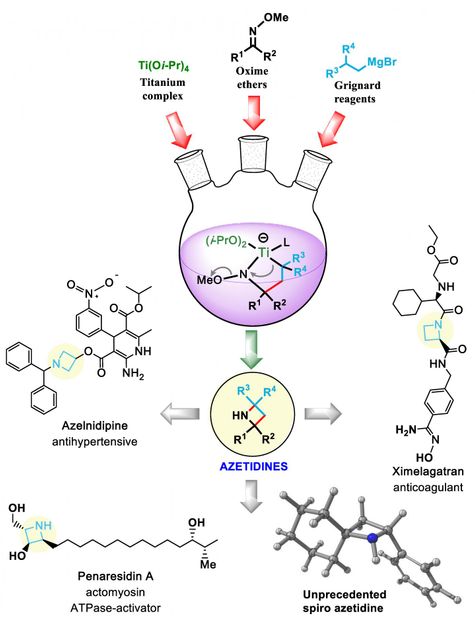
Los químicos de la Universidad de Rice desarrollaron una vía sintética hacia las azetidinas, moléculas que exponen átomos de nitrógeno que sirven como precursores para el diseño de drogas.
László Kürti/Rice University

Los nitrógenos son el punto. Los cuadrados son los marcos que los llevan. Estas moléculas se denominan azetidinas y se pueden utilizar como bloques de construcción en el diseño de fármacos.
El laboratorio del químico László Kürti introdujo sus azetidinas en un papel Angewandte Chemie. El objetivo del laboratorio es establecer una biblioteca de andamiajes para el diseño farmacéutico a través de la simple síntesis de una clase de moléculas que antes eran difíciles de encontrar en la naturaleza y muy difíciles de copiar.
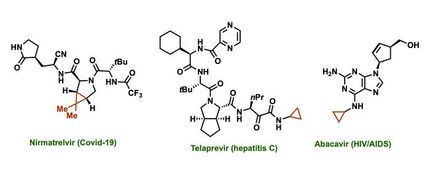
Las azetidinas ya aparecen en varios medicamentos y son componentes prometedores en el desarrollo de tratamientos para enfermedades neurológicas como la enfermedad de Parkinson, el síndrome de Tourette y el trastorno por déficit de atención, según los investigadores.
Por lo tanto, es valioso crear una ruta sintética rápida y económica hacia las azetidinas con átomos de nitrógeno sin protección llamados NH-azetidinas -- NH para nitrógeno e hidrógeno -- que se encontraron por primera vez en varios tipos de esponjas de mar del Pacífico y que más recientemente se han fabricado en arduos procesos de laboratorio.
Las estudiantes graduadas de Rice Nicole Behnke y Kaitlyn Lovato, autoras principales del artículo, aprendieron rápidamente por qué hay tan pocas referencias a las NH-azetidinas sintéticas en la literatura científica.
Se requirieron más de 250 experimentos para que los estudiantes optimizasen su proceso, lo cual toma alrededor de 24 horas, incluyendo la purificación del producto. Las moléculas de azetidina vienen en muchas configuraciones, pero todas comparten el motivo cuadrado, un "anillo" de cuatro átomos que contiene un átomo de nitrógeno y tres átomos de carbono. Este anillo es heterocíclico, es decir, contiene al menos dos elementos diferentes.
Kürti observó que el anillo cuadrado siempre está conectado a otro anillo a través de un átomo de carbono compartido, una estructura llamada espiroazetidina. De esta manera, los dos anillos son perpendiculares entre sí, aislando aún más el nitrógeno altamente reactivo para el acceso de los químicos. Las variaciones de nitrógeno en el laboratorio de Rice fueron a menudo, aunque no siempre, emparejadas con una"tapa" de átomo de hidrógeno que todavía permite que el nitrógeno reaccione con agentes externos.
"El Dr. Kürti se inspiró en el mecanismo de un proceso sintético llamado reacción Kulinkovich, que se utiliza para fabricar anillos de carbono de tres miembros, llamados ciclopropanos, que tienen el heteroátomo (el nitrógeno u oxígeno) en el exterior", dijo Lovato.
"Una vez que comenzamos a buscar la fabricación de azetidinas de cuatro miembros, descubrimos que la mayoría de ellos no tenían las estructuras de NH", dijo. "Los métodos sintéticos conocidos producen predominantemente azetidinas en las que el átomo de nitrógeno en anillo está conectado a un carbono fuera del anillo, pero la conectividad de NH era difícil de acceder directamente. Si hay un carbono allí, el nitrógeno se considera protegido, pero tener el hidrógeno allí lo deja libre para participar en otras reacciones".
"Una vez que se hace este heterociclo de NH, se tiene la flexibilidad de poner lo que se quiera en el nitrógeno", dijo Kürti. "O dejarlo como está."
Un reactivo de titanio resultó ser un intermediario clave en la reacción química, lo que le permitió proceder rápidamente. "Este complejo metálico media la transformación general, y es muy bueno porque el titanio no es tóxico y es muy abundante", dijo.
"Está disponible en el mercado y es barato", dijo Behnke. "Si no le agregamos titanio al frasco, la reacción no funciona."
El equipo de Rice no patentó el proceso, dijo Kürti. "La realidad es que los químicos orgánicos sintéticos en el mundo académico pueden contribuir mucho a las ciencias biomédicas y al descubrimiento de fármacos cuando desarrollamos un nuevo mecanismo o reacción", dijo.
"Las compañías biotecnológicas y farmacéuticas pueden utilizar los productos de estas reacciones para construir bibliotecas de compuestos estructuralmente diversos y someterlos rápidamente a pruebas para detectar actividades biológicas en diferentes líneas celulares de cáncer, patógenos u otras vías bioquímicas importantes de la enfermedad para las que tienen ensayos", dijo Kürti. "Una vez que tienen acceso a nuevas estructuras centrales como estas espiro azetidinas, es decisión de los químicos médicos decidir qué funcionalidades diversas desean añadir."
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.