Un paso más hacia las pilas de estado sólido
Sin necesidad de sinterización: síntesis a baja temperatura de cerámica de litio para baterías
Anuncios
Una cerámica de litio podría actuar como electrolito sólido en una generación más potente y rentable de baterías recargables de iones de litio. El reto es encontrar un método de producción que funcione sin sinterización a altas temperaturas. En la revista Angewandte Chemie, un equipo de investigadores ha presentado ahora un método sin sinterización para la síntesis eficiente y a baja temperatura de estas cerámicas en forma cristalina conductora.
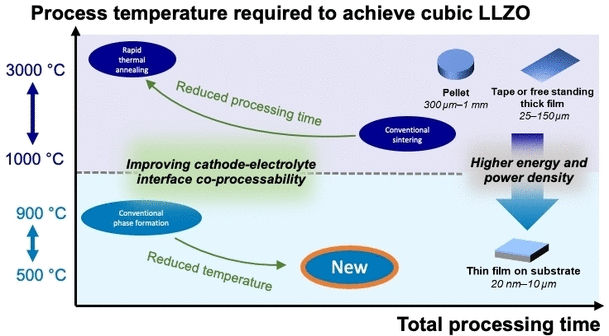
© Wiley-VCH
Dos factores dominan el desarrollo de baterías para vehículos eléctricos: la potencia, que determina la autonomía del vehículo; y el coste, crítico en la competencia con los motores de combustión interna. El Departamento de Energía de EE.UU. pretende acelerar la transición de los vehículos de gasolina a los eléctricos y ha fijado ambiciosos objetivos para reducir los costes de producción y aumentar la densidad energética de las baterías de aquí a 2030. Estos objetivos no pueden alcanzarse con las baterías convencionales de iones de litio.
Un enfoque muy prometedor para fabricar baterías más pequeñas, ligeras, mucho más potentes y seguras consiste en utilizar celdas de estado sólido con ánodos de litio metálico en lugar de grafito. A diferencia de las baterías de iones de litio convencionales, que tienen electrolitos orgánicos líquidos y utilizan una película de polímero para separar los compartimentos anódico y catódico, todos los componentes de una batería de estado sólido son sólidos. Una fina capa cerámica funciona simultáneamente como electrolito sólido y separador. Es muy eficaz tanto contra los peligrosos cortocircuitos causados por el crecimiento de dendritas de litio como contra el desbordamiento térmico. Además, no contienen líquidos fácilmente inflamables.
Un electrolito/separador cerámico adecuado para las pilas de alta densidad energética es el óxido de litio tipo granate Li7La3Zr2O12-d (LLZO). Este material debe sinterizarse junto con el cátodo a más de 1050 °C para convertir el LLZO en la fase cristalina cúbica conductora rápida del litio, densificarlo suficientemente y unirlo fuertemente al electrodo. Sin embargo, las temperaturas superiores a 600 °C desestabilizan los materiales catódicos sostenibles bajos en cobalto o sin cobalto, al tiempo que aumentan los costes de producción y el consumo de energía. Se necesitan nuevos métodos de producción más económicos y sostenibles.
Un equipo dirigido por Jennifer L. M. Rupp, del MIT de Cambridge (EE.UU.) y la Universidad Técnica de Múnich (Alemania), ha desarrollado un nuevo proceso sintético. Su nuevo proceso no se basa en un compuesto precursor cerámico, sino en uno líquido, que se densifica directamente para formar LLZO en una síntesis de descomposición secuencial. Para optimizar las condiciones de esta ruta sintética, Rupp y su equipo analizaron la transformación de fase multietapa del LLZO desde una forma amorfa hasta la forma cristalina requerida (cLLZO) utilizando diversos métodos (espectroscopia Raman, calorimetría diferencial dinámica de barrido) y elaboraron un diagrama de tiempo-temperatura-transformación. Basándose en los conocimientos adquiridos sobre el proceso de cristalización, desarrollaron una ruta por la que el cLLZO se obtiene como una película densa y sólida tras 10 horas de recocido a la temperatura relativamente baja de 500 °C, sin sinterización. Para futuros diseños de baterías, este método permitirá integrar el electrolito sólido LLZO con cátodos sostenibles que podrían evitar el uso de elementos socioeconómicamente críticos como el cobalto.
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Inglés se puede encontrar aquí.