La ciencia de los materiales se une a la medicina: por qué fallan los implantes
Anuncios
¿Qué ocurre con los implantes de titanio en el organismo? ¿Por qué a veces son rechazados o incluso se rompen? La investigadora de Empa Martina Cihova busca respuestas a estas preguntas en la interfaz entre el implante y el cuerpo, entre la ciencia de los materiales y la medicina. Recientemente ha recibido una "Beca Ambizione" de la Fundación Nacional Suiza para la Ciencia (FNS) para su proyecto de investigación.

La investigadora del Empa Martina Cihova investiga cómo el organismo puede atacar la superficie de los implantes de titanio.
Empa

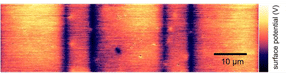
La imagen del microscopio de fuerza atómica muestra zonas claramente reconocibles con diferentes potenciales superficiales, creados por cambios inducidos por láser en la estructura del óxido de titanio.
Empa

Gracias a los avances médicos, cada vez vivimos más años. Es comprensible que queramos mantenernos sanos y móviles hasta una edad avanzada. Los implantes y prótesis sustituyen a las articulaciones y dientes "desgastados", acaban con el dolor y mejoran la calidad de vida. Los implantes médicos modernos son pequeñas maravillas de biomaterial y bioingeniería al mismo tiempo. Sin embargo, en ocasiones los implantes fallan, lo que puede tener graves consecuencias para los pacientes.
¿Por qué se producen estos fallos y por qué han aumentado en lugar de disminuir en los últimos años? La investigadora de Empa Martina Cihova, del laboratorio "Tecnología de unión y corrosión", quiere dar respuesta a estas preguntas. Para ello, está observando de cerca el comportamiento de los implantes en el cuerpo o, para ser más precisos, bajo el microscopio. La científica ha recibido una "Beca Ambizione" de cuatro años de la Fundación Nacional Suiza para la Ciencia para su proyecto de investigación.
Muchos implantes, como las articulaciones artificiales, los implantes dentales y los marcapasos, están hechos de titanio. Este metal de transición es ligero y estable, muy duradero en el cuerpo y permite que el hueso crezca especialmente bien. Estas propiedades se deben a una fina capa de óxido que se forma en la superficie del titanio cuando entra en contacto con el aire. En última instancia, no es el titanio en sí, sino la capa protectora de la superficie de los implantes la que entra en contacto con el cuerpo. "Como esta capa pasiva natural tiene menos de diez nanómetros de grosor, a menudo recibe muy poca atención en la tecnología y la investigación médicas", afirma Martina Cihova.
Además, algunos fabricantes modifican la capa de óxido, por ejemplo engrosándola para dar a los distintos tamaños o modelos de implantes un código de colores y facilitar así el trabajo a los médicos. Otros hacen más rugosa la superficie de los implantes para que el hueso crezca mejor, o graban el número de serie con láser. La impresión en 3D de implantes específicos para cada paciente también es posible hoy en día mediante procesos láser. Todas son aplicaciones sensatas, pero: "Cualquier tratamiento superficial puede cambiar los óxidos de titanio de la superficie", dice Cihova, "y se ha investigado muy poco lo que esto significa para la interacción del implante con el cuerpo y para su resistencia a la corrosión".
Investigación en la frontera
La investigadora de Empa quiere colmar esta laguna de conocimientos con su proyecto. Ya como estudiante de bioingeniería, a Cihova le entusiasmaba la ciencia de los materiales. Por eso emprendió un nuevo camino en su doctorado -la metalurgia- para profundizar en su interés por los materiales. Ahora combina sus conocimientos en los dos campos y los centra precisamente en el punto de encuentro entre el metal, o los óxidos metálicos, y la biología: la interfaz entre el implante y el cuerpo humano.
"Estas biointerfaces son muy complejas, pero también sumamente interesantes", afirma la joven investigadora. "Cuando uno piensa en la corrosión, piensa en el agua salada del mar, en el aire húmedo, quizá en una bicicleta oxidada... pero no en el cuerpo humano". Sin embargo, el cuerpo humano puede ser un entorno sorprendentemente agresivo, sobre todo cuando se producen reacciones inmunitarias. Las células inmunitarias liberan diversas sustancias que pueden, entre otras cosas, reducir el valor del pH y atacar el implante. Entonces, ¿qué hace el cuerpo con materiales que consideramos estables? Aquí es precisamente donde entra en juego la investigación sobre la biocorrosión.
Estos procesos son muy complejos a nivel (electro)químico y biológico. Además, no todo el óxido de titanio es igual. Puede adoptar tres formas cristalinas diferentes -todas con la misma composición química, TiO2- o ser amorfo, estructuralmente "indefinido", por así decirlo. Todas estas formas difieren en sus propiedades electrónicas y electroquímicas y, por tanto, potencialmente también en sus interacciones con el organismo.
Aumentar la complejidad de forma controlada
El tratamiento superficial de los implantes puede cambiar las formas cristalinas de los óxidos, ya sea en todo el implante o sólo de forma selectiva. Se necesita un enfoque estructurado para comprender los efectos de esta heterogeneidad local, sobre todo en la ya compleja biointerfaz. En primer lugar, Cihova y su equipo, en colaboración con los expertos de Empa para el procesamiento láser de metales en Thun, producen sustratos de muestra con capas de óxido de titanio de estructura diferente que varían sistemáticamente en su heterogeneidad. A continuación, estos sustratos se exponen sucesivamente a fluidos corporales cada vez más complejos para investigar las relaciones fundamentales entre la estructura, las propiedades y la reactividad de los óxidos.
"Empezamos con fluidos fisiológicos simulados que sólo contienen agua e iones", explica Cihova. El siguiente paso será añadir proteínas, como el fibrinógeno, que interviene en la respuesta inmunitaria y la cicatrización de heridas. Por último, los investigadores planean estudiar cómo se comporta la biointerfaz en contacto con células macrófagas vivas, los "policías del cuerpo". Para ello colaboran con investigadores del Empa de St. "Estoy muy contenta de que hayamos podido implicar en este proyecto a colegas de las tres sedes de Empa", afirma Cihova. "Esto nos permite abordar cuestiones tan complejas de forma interdisciplinaria".
En cada uno de estos pasos, las interfaces se examinan "a fondo" utilizando métodos electroquímicos combinados con microscopía de fuerza atómica y electrónica de alta resolución. "Ver es comprender, aunque sea a una escala mucho menor que la de una célula humana", explica Cihova. "Ahí es donde a menudo pueden descubrirse detalles cruciales".
La investigadora del Empa espera que los hallazgos de los próximos años conduzcan a implantes más seguros y estables. Y también "que aprendamos más sobre cómo la fascinante gama de propiedades del óxido puede utilizarse específicamente en biomedicina". Tras su proyecto "Ambizione" en 2028, también quiere extender los nuevos métodos a otros materiales médicos. Cihova está convencida de que este campo de investigación cobrará aún más importancia en el futuro: "El comportamiento de los óxidos metálicos en las biointerfaces también es clave para su rendimiento en los campos emergentes de la nanomedicina y la tecnología de sensores implantables."
Nota: Este artículo ha sido traducido utilizando un sistema informático sin intervención humana. LUMITOS ofrece estas traducciones automáticas para presentar una gama más amplia de noticias de actualidad. Como este artículo ha sido traducido con traducción automática, es posible que contenga errores de vocabulario, sintaxis o gramática. El artículo original en Alemán se puede encontrar aquí.













































