El titanio es un elemento químico, de símbolo Ti y número atómico 22. Se trata de un metal de transición de color gris plata. Comparado con el acero, con quien compite en aplicaciones técnicas, es mucho más ligero (4,5/7,8). Tiene alta resistencia a la corrosión y gran resistencia mecánica, pero es mucho más caro que el acero, lo cual limita su uso industrial. Es un metal abundante en la naturaleza; se considera que es el cuarto metal estructural más abundante en la superficie terrestre y el noveno en la gama de metales industriales. No se encuentra en estado puro sino en forma de óxidos, en la escoria de ciertos minerales de hierro y en cenizas de animales y plantas. Su utilización se ha generalizado con el desarrollo de la tecnología aeroespacial, donde es capaz de soportar las condiciones extremas de frío y calor que se dan en el espacio y en la industria química, por ser resistente al ataque de muchos ácidos; asimismo, este metal tiene propiedades biocompatibles, porque los tejidos del organismo toleran su presencia y por tanto permite fabricar muchas prótesis e implantes de este metal. Posee propiedades mecánicas parecidas al acero, tanto puro como en las aleaciones que forma. Y por tanto compite con el acero en muchas aplicaciones técnicas, especialmente con el acero inoxidable. El titanio fue declarado material estratégico por parte Estados Unidos durante muchos años. Puede formar aleaciónes con otros elementos, tales como hierro, aluminio, vanadio, molibdeno y otros, para producir componentes muy resistentes que son utilizados por la industria aeroespacial, aeronáutica, militar, petroquímica, agroindustrial, automovilística y médica. Producto destacadoHistoriaEl titanio (llamado así por los Titanes, hijos de Urano y Gea en la mitología griega) fue descubierto en Inglaterra por William Gregor, en 1791, cuando estudiaba un metal de color gris-plata que había encontrado. Poco después, en 1795, el químico austríaco Martín Kalprotz, descubridor también del uranio, le dio el nombre de titanio. Este elemento es, en cuanto a su abundancia, el noveno de los que forman la corteza terrestre. Virtualmente, todas las rocas ígneas, y sus sedimentos, así como muchos minerales, principalmente los que contienen hierro y todos los organismos vegetales y animales, contienen titanio. El mineral más importante del que se extrae titanio es el rutilo (óxido de titanio), muy abundante en las arenas costeras. Por su parte el titanio debe ser sometido previamente a un proceso metalúrgico de refinado, para prevenir su eventual reacción con sustancias gaseosas, tales como el nitrógeno, el oxígeno y el hidrógeno. Matthew A. Hunter preparó por primera vez titanio metálico puro (con una pureza del 99.9%) calentando tetracloruro de titanio (TiCl4) con sodio a 700-800 °C en un reactor de acero. El titanio como metal no se usó fuera del laboratorio hasta que en 1946 William Justin Kroll desarrolló un método para poder producirlo comercialmente, mediante la reducción del TiCl4 con magnesio, y este método, llamado Método de Kroll, es el utilizado aún hoy en día (2008). En este proceso el metal se mantiene constantemente en una atmósfera de gas inerte, como argón o helio, que inhibe la reacción con cualquier otro elemento.[1] Durante los años 50 y 60 la Unión Soviética promovió el empleo de titanio en usos militares y submarinos (Clase Alfa y Clase Miguel) como parte de sus programas militares relacionados con la guerra fría. En los EE. UU., el Departamento de Defensa (DOD) comprendió la importancia estratégica del metal y apoyó los esfuerzos para su comercialización. A lo largo del período de la guerra fría, el gobierno estadounidense consideró al titanio como un material estratégico, y las reservas de esponja de titanio fueron mantenidas por el Centro de Reservas Nacional de Defensa, que desapareció en 2005. Hoy el mayor productor mundial es el consorcio ruso VSMPO-AVISMA, que representa aproximadamente el 29% de la cuota mundial de mercado. En 2006, la Agencia de Defensa estadounidense concedió 5,7 millones de dólares a un consorcio de dos empresas para desarrollar un nuevo proceso para fabricar polvo de metal de titanio. Bajo calor y presión, se puede usar el polvo para crear artículos fuertes, de peso ligero en las superficies de revestimiento de armaduras o componentes para el espacio aéreo, el transporte e industrias de tratamiento químico. IsótoposSe encuentran 5 isótopos estables en la naturaleza: 46Ti, 47Ti, 48Ti, 49Ti y 50Ti, siendo el 48Ti el más abundante (73,8%). Se han caracterizado 11 radioisótopos, siendo los más estables el 44Ti, con un periodo de semidesintegración de 60.0 años, 45Ti (184.8 minutos), 51Ti (5.76 minutos) y el 52Ti (1,7 minutos). Para el resto, sus periodos de semidesintegración son de menos de 33 segundos, y la mayoría de menos de medio segundo. El peso atómico de los isótopos va desde 39,99 uma (40Ti) hasta 57,966 uma (58Ti). El primer modo de decaimiento antes del isótopo más estable, el 48Ti, es la captura electrónica, mientras que después de éste es la desintegración beta. Los isótopos del elemento 21 (escandio) son los principales productos de decaimiento antes del 48Ti, mientras que después son los isótopos del elemento 23 (vanadio).[2] Características del titanioCaracterísticas físicasEntre las características físicas del titanio se tienen las siguientes:
Características mecánicasEntre las características mecánicas del titanio se tienen las siguientes:
Características químicas
Metalurgia del titanio: El método KrollEl titanio no se encuentra libre en la Naturaleza, los minerales que muestran una mayor concentración de este metal son el rutilo (TiO2) y la ilmenita(FeO•TiO2), además de la anatasa y la brookita (ambas son también TiO2). Para obtener titanio puro, a partir de los minerales que lo contienen se utiliza mayoritariamente el llamado Método de Kroll, que consiste en la reducción del compuesto tetracloruro de titanio con magnesio molido, en una atmósfera de argón para evitar la oxidación. El proceso consta de los siguientes pasos:
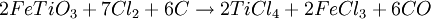
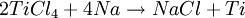

En la actualidad (2007) existen varios proyectos de refinado del titanio, como alternativa al método Kroll, tradicionalmente utilizado desde 1937. Aleaciones de titanioComercial y técnicamente existen muchas aleaciones de titanio porque no hay una norma muy rígida sobre las mismas. Sin embargo las aleaciones más conocidas son las siguientes y se conocen por el grado que tienen. Ti grado 2, tiene la siguiente composición química: TiFe(0,25-0,30) Es conocido como titanio comercial puro. Tiene una resistencia a la tracción de 345 MPa, un límite elástico de 275 MPa, una ductilidad del 20% una dureza de 82 HRB una excelente soldadura y una resistencia eléctrica de 0,56 (μΩm). Sus principales aplicaciones son donde se requiere resistencia a la corrosión y conformabilidad ( Tuberías, intercambiadores de calor,etc) Ti grado 5, tiene la siguiente composición química: Ti6Al4V Tiene una resistencia a la tracción de 896 MPa, un límite elástico de 827 MPa, una ductilidad del 10% una dureza de 33 HRB una soldabilidad muy buena y una resistividad eléctrica de 1,67 (μΩm). Sus aplicaciones son donde se requiera alta resistencia mecánica y altas temperaturas ( Tornillería y piezas forjadas) Ti grado 19, tiene la siguiente composición química Ti3Al8V6Cr4Zr4Mo (Beta-C) Tiene una resistencia a la tracción de 793 MPa, un límite elástico de 759 MPa una ductilidad de 15% una dureza de 45 HRB una soldabilidad regular y una resistividad de 1,55 (μΩm). Sus aplicaciones son donde se requiera alta resistencia a la corrosión y a la temperatura ((Aplicaciones marinas y motores de aviones) Ti6246 Tiene la siguiente composición química: Ti6Al2Sn4Zr6Mo, Tiene una resistencia a la tracción de 1172 Mpa, un límite elástico de 1103 Mpa una ductilidad del 10% una dureza de 39 HRB una soldabilidad limitada y una resistividad eléctrica de 2 (μΩm) Sus aplicaciones son donde se requiera alta resistencia mecánica obtenida por temple.
Los más utilizados son los siguientes:
La aleación Ti Beta-C es una aleación con alta resistencia a la corrosión y a la temperatura. Las siguientes aleaciones muestran sus utilidades principales:
Los productos consumibles de soldadura son amparados por la especificación AWS A5.16.[4] Procesos tecnológicos del titanioFundiciónLa fundición de piezas de titanio se realiza cuando se trata de piezas de diseño complejo que hace difícil el forjado o mecanizado de las mismas. Hay muchas aplicaciones donde se utilizan piezas fundidas desde piezas muy voluminosas hasta piezas muy pequeñas de aplicaciones biomédicas. Hay dos métodos principales para la fundición de piezas:
En el desarrollo de las diferentes prótesis óseas y dentales se recurre a la fundición de los componentes en hornos muy sofisticados para obtener una gran precisión y calidad de las piezas fundidas, a partir de los moldes adecuados. Debido a la afinidad del titanio líquido por el oxígeno, nitrógeno e hidrógeno, así como la reactividad con los crisoles y moldes metálicos, se requiere que la fusión sea al vacío y en crisoles de grafito. Las propiedades mecánicas de las piezas de fundición son muy similares a las de las piezas forjadas y del titanio en general. Se funden piezas de hasta 600 Kg, tanto de titanio comercial puro como de las diferentes aleaciones. La verificación de piezas fundidas se realiza mediante líquidos penetrantes, rayos X o ultrasonidos.[5] ForjaPara la conformación de piezas de titanio por forjado se pueden utilizar las técnicas y herramientas convencionales que se utilizan para el forjado de piezas de acero. El forjado en caliente exige controlar rigurosamente la temperatura con la que se trabaja, para obtener un control exacto de la estructura de la pieza y de sus propiedades. Se pueden forjar piezas de cualquier aleación de titanio con estructura de grado único y con una resistencia y dureza direccionales o localizadas. Las modernas máquinas herramientas de mecanizado por Control Numérico está eliminando muchas veces el forjado de piezas cuando se trata de series reducidas porque es más económico realizar un mecanizado de desbaste general de la pieza y un posterior acabado fino que un proceso de forja La posibilidad de la deformación en caliente si se hace a temperatura superior a la transformación alotrópica que es equivalente a la de los aceros inoxidables, puede presentar en algunos casos superelasticidad. Ejemplo de piezas forjadas pueden ser las siguientes:
SoldaduraA la hora de afrontar la soldadura de piezas de titanio hay que tener en cuenta que si se supera la temperatura de fusión, puede sufrir una decoloración porque reacciona fácilmente en contacto con los gases atmosféricos. Esta decoloración puede suponer pérdida de ductilidad y de resistencia mecánica. Por lo tanto es muy importante que en la soldadura se proteja la zona de soldadura con gases inertes. También perjudican la soldadura los contaminantes de las superficies a soldar, tales como óxido, polvo, limaduras y virutas, por lo que deben eliminarse por baño de decapación, mecanizado pulido o chorro de arena. la soldadura debe limpiarse con paño de acetona, o cepillo de acero inoxidable o titanio El titanio de grado 2 y 5 poseen una buena soldabilidad aunque pierden un poco de valor de sus propiedades mecánicas con respecto al metal base. El equipo de soldadura con arco de gas inerte para titanio (TIG, MIG) es similar a los equipos utilizados para soldar acero, aunque se requiere una mejor protección del gas inerte. En caso de piezas críticas donde la protección gaseosa sea difícil puede ser necesario realizar la soldadura en una cámara de soldadura. Para la verificación de piezas soldadas se puede recurrir a los métodos tradicionales de rayos X, ultrasonidos o líquidos penetrantes. Los procesos de soldadura que admite el titanio son:
ExtrusiónExtrusión es, en general, la acción de dar forma o moldear una masa haciéndola salir por una abertura especialmente dispuesta El titanio y sus aleaciones permiten ser extruidos, pudiendo obtener diversos perfiles tanto para acabados en bruto como para piezas finales. La técnica de extrusión es particularmente recomendable para la producción de pieza largas y de sección compleja. EmbuticiónLa embutición es una técnica de moldeo de metales en caliente que permite fabricar piezas complejas en un sola operación con la acción conjunta de una prensa y el molde o troquel adecuado a la pieza que se quiere fabricar. Para facilitar la embutición es necesario que el material tenga una gran elongación a la tracción. que se trate de materiales policristalinos da grano fino a altas temperaturas. Esta propiedad la tiene la aleación de titanio de grado 5 Ti6Al4V. La técnica consiste colocar la pieza a moldear entre las dos mitades del troquel o molde, a la temperatura que permita la mejor superplasticidad del material. Se insufla argón caliente en la parte superior del molde y se fuerza la lámina de titanio contra la parte interior del troquel. Esta técnica es adecuada solo para lotes de piezas muy grandes, dado la carestía de los troqueles y moldes, pero tiene la ventaja de que el tiempo de conformación de la pieza es muy corto, reduciendo así el periodo de lanzamiento del producto, así como eliminado tareas de mecanizado posteriores y reduciendo la cantidad de materia prima utilizada. MecanizadoEl mecanizado de piezas de titanio en máquinas herramientas normales se realiza en condiciones parecidas a las que se utiliza para mecanizar acero inoxidable o aleaciones de aluminio, y las condiciones tecnológicas del mecanizado dependerán de la dureza que tenga la aleación de titanio que se mecanice. El titanio posee un módulo de elasticidad menor que el del acero y por tanto es más elástico por lo que las piezas pueden tender a doblarse. Hay que refrigerar el mecanizado con un refrigerante adecuado teniendo en cuenta que el titanio es mal conductor térmico y por tanto difícil de refrigerar, pudiendo deteriorar el filo de corte de las herramientas a consecuencia de las altas temperaturas en la zona de corte. Fresado químicoLas piezas de titanio permiten el fresado químico de tal manera que se puede conseguir una gran precisión en dicha operación. Para esta tarea se utiliza un ataque de ácido de superficie, selectivo y controlado. Las zonas de material que no deben ser fresadas se protegen con una capa de elastómero de neopreno o de copolímero de isobutileno-isopropileno. Rectificado de precisiónLos rectificados de precisión deben realizarse con muelas abrasivas muy reavivadas, con el mayor diámetro y espesor posible, duras y con gran potencia y velocidades lineales adecuadas. Para el rectificado cilíndrico se recomiendan muelas con alúmina y un refrigerante adecuado de chorro de gran caudal que sea muy bien filtrado y cambiarlo a menudo. PulvimetalurgiaLa pulvimetalurgia o metalurgia de polvos es un proceso de fabricación que, partiendo de polvos finos y tras su compactación para darles una forma determinada (compactado), se calientan en atmósfera controlada (sinterizado) para la obtención de la pieza. La pulvimetalurgia del titanio se utiliza para la fabricación de piezas complejas de espesores muy pequeños, por ejemplo menores de 1 mm, donde se exijan acabados superficiales muy finos. Se puede conseguir pulvitanio de base mediante las siguientes técnicas:
Tratamientos del titanioTratamiento termoquímico: NitruraciónEl tratamiento termoquímico de nitruración del titanio puro y de la aleación Ti6Al4V produce una capa lisa y homogénea , con incrementos de la dureza superficial de hasta un 500% respecto al material no tratado. La capa de nitruros formada tiene un espesor de 2-3 mm, en tres horas de tratamiento, formada por pequeños granos de nitruros con diámetros del orden de los 50-100 nm. El componente principal de la capa es nitruro de titanio (Ti2N) Este tipo de tratamiento tiene gran utilidad en las aplicaciones biomédicas del titanio y en los componentes de motocicletas y automóviles de competición: bielas, válvulas, etc.[6] Las piezas a tratar se colocan en una cámara en vacío y son sometidas a una temperatura de 500 ºC. Se inyecta nitrógeno, que en contacto con iones de titanio, reaccionan para formar nitruro de titanio, presentando al final del proceso un color dorado. Con esta técnica la dureza superficial puede aumentar hasta 2600 HRB. las piezas nitruradas tienen una gran resistencia a la corrosión. Tratamiento superficialComo tratamientos superficiales del titanio se pueden citar los siguientes:
Cuando se produce deslizamiento de superficies de titanio sobre titanio o cualquier otro metal, se manifiesta una gran tendencia a la excoriación, por lo que se requiere en esos casos lubricar las superficies de contacto con lubricantes de película seca a base de disulfuro de molibdeno, grafito o similares. Donde más se aplica este tipo de lubricación es en tornillos y pernos roscados. Un método de mejorar las propiedades superficiales del titanio, concretamente la mejora de la resistencia a la corrosión, es cuando se somete el titanio a un tratamiento superficial de oxidación que, además, puede originar una variedad de colores muy atractiva que amplía las posibilidades del titanio en el sector de la joyería y de la decoración. Existen distintas técnicas para llevar a cabo la oxidación superficial del titanio para producir su coloración, como son el tratamiento térmico, el procesado con plasma o la oxidación electrolítica. Ya existe una alternativa a los métodos tradicionales de oxidación que consiste en que el tratamiento superficial se realice con láser. Esta técnica presenta una gran resolución espacial, rapidez de procesado y ausencia de contacto material con la pieza a tratar. Además, la posibilidad de irradiar zonas de difícil acceso y la versatilidad de los sistemas de marcado proporcionan al láser una gran aplicabilidad en la coloración del titanio. El proceso de láser también puede ser empleado posteriormente al proceso de anodizado para escribir, grabar y marcar.[7] El proceso de anodización es una técnica que se utiliza para aumentar el grosor de la capa de óxido y constituye una solución eficaz y poco costosa para piezas que no estén sometidas a un desgaste continuo. Si durante la anodización se depositan polímeros de bajo coeficiente de rozamiento se aumenta la dureza superficial de la pieza. El tratamiento superficial de ionización se realiza en frío y consiste en acelerar en vacío iones de nitrógeno y hacerlos impactar contra la superficie tratada. Con este procedimiento la dureza superficial aumenta hasta 1500 HV. esta técnica da muy buenos resultados en el tratamiento de engranajes y tornillería. Aplicaciones del titanioAplicaciones biomédicas: Titanio quirúrgicoEl titanio es un metal biocompatible, porque los tejidos del organismo toleran su presencia sin que se hayan observado reacciones alérgicas del sistema inmunitario. Esta propiedad de biocompatibilidad del titanio unido a sus cualidades mecánicas de dureza, ligereza y resistencia han hecho posible una gran cantidad de aplicaciones de gran utilidad para aplicaciones médicas, como prótesis de cadera y rodilla, tornillos óseos, placas antitrauma e implantes dentales, componentes para la fabricación de válvulas cardíacas y marcapasos, gafas, herramental quirúrgico tales como bisturís, tijeras, etc., y también la gran cantidad de piezas llamadas piercing.
Las especificaciones de ASTM para el titanio quirúrgico son las siguientes:
quirúrgico
Las razones para considerar el material ideal para implantes endoóseos son:
Esta reacción normalmente sólo se presenta en los materiales llamados bioactivos y es la mejor base para los implantes dentales funcionales.
Otros usos
Aplicaciones del titanio no metálicoAlgunos compuestos de titanio pueden tener aplicaciones en tratamientos contra el cáncer. Por ejemplo, el cloruro de titanoceno en el caso de tumores gastrointestinales y de mama. Tetracloruro de titanioEl tetracloruro de titanio (TiCl4)es un líquido incoloro que tiende a amarillo pálido que emite vapores de olor fuerte. Si entra en contacto con agua, rápidamente forma ácido clorhídrico, como también compuestos de titanio. El tetracloruro de titanio no se encuentra de forma natural en el medio ambiente y es producido por un proceso químico a partir de los minerales que contienen titanio. Es usado para fabricar titanio metálico y otros compuestos que contienen titanio, tales como bióxido de titanio. También se usa para irisar el vidrio y, debido a que en contacto con el aire forma mucho humo, se emplea para formar artificialmente pantallas de humo. Se emplea para obtener piedras preciosas artificiales.[10] El (TiCl4) se obtiene mediante un proceso de cloración a 800 ºC, en presencia de carbono(C) mediante la reacción: 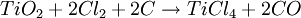 Posteriormente si se desea obtener titanio puro se purifica este producto con magnesio (Mg) o sodio molido (Na) mediante destilación fraccionada en una atmósfera inerte (por ejemplo con argón) con la reacción: Si se utiliza el Sodio (Na) en el proceso se producen la siguiente reacción: 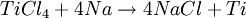 Si se utiliza Magnesio (Mg) se producen la siguiente reacción:  Para manejar este producto hay que tomar precauciones porque entra en el ambiente principalmente en el aire de las instalaciones industriales donde se produce mediante una variedad de procesos químicos, o como resultado de derrames. Si hay humedad en el aire, el tetracloruro de titanio reacciona rápidamente con ésta para formar ácido clorhídrico y otros compuestos de titanio, tales como el hidróxido de titanio y los oxicloruros de titanio. Algunos de los compuestos de titanio pueden depositarse en el suelo o el agua. En el agua, estos se depositan en el sedimento del fondo donde pueden permanecer por largo tiempo. El tetracloruro de titanio se degrada rápidamente en el aire, por lo que no es tóxico a menos que trabaje en una industria que lo manufactura o lo usa. El personal que trabaja en una industria que usa tetracloruro de titanio, podría estar expuesto respirándolo o tocándolo. Si se derrama tetracloruro de titanio, puede haber contacto con la piel. El tetracloruro de titanio es muy irritante a los ojos, la piel, membranas mucosas y los pulmones. Respirar grandes cantidades puede causar serios daños a los pulmones. El contacto con el líquido puede causar quemaduras a los ojos y la piel. Dióxido de titanio
El dióxido de titanio es un compuesto cuya fórmula es (TiO2).Se encuentra en una forma negra o de color castaño conocida como rutilo. Las formas naturales que se encuentra menos en la naturaleza son la anatasita y la brooquita.Tanto el rutilo como la anatasita puros son de color blanco. El óxido básico negro, (FeTiO3), se encuentra en forma natural como el mineral llamado ilmenita. El dióxido de titanio es la principal fuente comercial del titanio. Aproximadamente el 95% del titanio que se consume lo hace en forma de dióxido de titanio, debido a las múltiples aplicaciones industriales que tiene. Propiedades
Aplicaciones
ProducciónEl dióxido de titanio es el pigmento blanco más importante producido en el mundo, con unas ventas anuales aproximadas de 4 millones de toneladas y un consumo mundial que aumenta en torno a un 2% anual (2004). Los principales usuarios son las industrias de pinturas y plásticos. Por cada tonelada de dióxido de titanio fabricado se producen casi 3,8 toneladas de productos derivados. En general, aproximadamente la mitad de estos productos derivados son vendidos, reutilizados o convertidos en otros productos como materia prima en aplicaciones como tratamiento de aguas, prefabricados de yeso, agricultura, cemento y tratamiento de terrenos. Los productos derivados para los cuales no puede encontrarse un mercado son entregados a gestores autorizados para su tratamiento mediante procedimientos ecológicos controlados.[13] Productores mundiales de titanioPrincipales productores de óxido de titanio en 2003
Cifras del 2003, en miles de toneladas de dióxido de titanio. Fuente: L'état du monde 2005, annuaire économique géopolique mondial El titanio es el noveno elemento más abundante en la corteza terrestre (supone el 0,63% del peso total). Sin embargo, en la naturaleza siempre se encuentra unido químicamente a otros elementos, formando minerales en los que la fracción de titanio suele ser pequeña. De todos los minerales de titanio, solo el rutilo y la ilmenita son explotables económicamente y esto sólo cuando la concentración de titanio es suficientemente alta. Existen depósitos significativos de titanio en forma de ilmenita en Australia occidental, Canadá, Nueva Zelanda, Noruega y Ucrania. Se extraen grandes cantidades de rutilo en Norteamérica y Sudáfrica. Las reservas conocidas de titanio se estiman en unas 600 millones de toneladas (expresadas como TiO2). Titanio y toxicidadDebido a la biocompatibilidad del titanio no se han descubierto casos de toxicidad tanto en el titanio elemental como en el dióxido de titanio Se han detectado algunos efectos de la sobreexposición al polvo de titanio por lo que la inhalación del polvo puede causar tirantez y dolor en el pecho, tos, y dificultad para respirar. El contacto con la piel y los ojos puede provocar irritación. Vías de entrada: Inhalación, contacto con la piel, contacto con los ojos. Respecto a la cancerología que pueda tener, la agencia internacional para la investigación del cáncer (IARC) ha incluido el dióxido de titanio en el grupo 3 que consiste en que el titanio no es clasificable como elemento cancerígeno en los humanos (el agente no es clasificable con respecto a su carcinogenicidad en humanos).[14] Referencias y bibliografíaEste artículo incorpora material de http://www.lowde.com , que mediante una autorización permitió agregar contenido e imágenes del Manual de Titanio que incorpora en la web y publicarlos bajo licencia GFDL.
Véase tambiénEnlaces externosTitanio Sistema periódico
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Este articulo se basa en el articulo Titanio publicado en la enciclopedia libre de Wikipedia. El contenido está disponible bajo los términos de la Licencia de GNU Free Documentation License. Véase también en Wikipedia para obtener una lista de autores. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||







